Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(V_{dd}=165,84\left(ml\right)=0,16584\left(l\right)\\ n_{CuSO_4}=\dfrac{36}{160}=0,225\left(mol\right)\\ \rightarrow C_{M\left(CuSO_4\right)}=\dfrac{0,225}{0,16584}=1,36M\)

Khối lượng dung dịch C u S O 4 ban đầu:
m d d = V.D = 165,84.1,206=200(g)
Nồng độ % của dung dịch C u S O 4 :
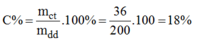

Theo de bai ta co
mddCuSO4=D.V=1,206.165,84\(\approx\)200 g
\(\Rightarrow\)Nong do % cua dd CuSO4 da dung la
C%=\(\dfrac{mct}{mdd}.100\%=\dfrac{36}{200}.100\%=18\%\)

Bài 6:
Từ 40oC \(\rightarrow\) 20oC
=> \(\Delta\)S = 60 - 15 = 45 ( gam )
Trong 160 g dung dịch bão hòa có khối lượng kết tinh là 45 gam
...........600.........................................................................x gam
=> x = \(\dfrac{600\times45}{160}\) = 168,75 ( gam )
1.
mKOH trong dd KOH 5%=400.\(\dfrac{5}{100}\)=20(g)
C% dd KOH=\(\dfrac{20+30}{400+30}.100\%=11,6\%\)

\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
0,2 0,2 0,2 ( mol )
\(m_{Cu}=0,2.64=12,8g\)
\(C_{M_{CuSO_4}}=\dfrac{0,2}{0,25}=0,8M\)

nHCl=0,6 mol
FeO+2HCl-->FeCl2+ H2O
x mol x mol
Fe2O3+6HCl-->2FeCl3+3H2O
x mol 2x mol
72x+160x=11,6 =>x=0,05 mol
A/ CFeCl2=0,05/0,3=1/6 M
CFeCl3=0,1/0,3=1/3 M
CHCl du=(0,6-0,4)/0,3=2/3 M
B/
NaOH+ HCl-->NaCl+H2O
0,2 0,2
2NaOH+FeCl2-->2NaCl+Fe(OH)2
0,1 0,05
3NaOH+FeCl3-->3NaCl+Fe(OH)3
0,3 0,1
nNaOH=0,6
CNaOH=0,6/1,5=0,4M

C% CuSO4 = \(\dfrac{32}{200}\).100% = 16%
Ta có ct:
CM = \(\dfrac{C\%.D.10}{M}\)=\(\dfrac{16.1,2.10}{160}\)= 1,2 M
Câu 1.
\(n_{H_2SO_4}=\frac{49}{98}=0,5\left(mol\right)\)
PTHH:
Zn + H2SO4 -------> ZnSO4 + H2 \(\uparrow\)
1___1mol_________1mol______1mol
0,2__0,5mol
Lập tỉ lệ : \(\frac{0,2}{1}< \frac{0,5}{1}\)
\(\Rightarrow\) H2SO4 dư, Zn hết
Theo pt \(\Rightarrow n_{H_2}=n_{Zn}=0,2\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,2\cdot22,4=4,48\left(l\right)\)
Câu 2.
Khối lượng của dung dịch CuSO4 ban đầu:
\(m_{dd}=1,206\cdot165,84\approx200\left(g\right)\)
Nông độ phầm trăm của dung dịch CuSO4 ban đầu:
\(C\%=\frac{36\cdot100\%}{200}=18\%\)
Câu 1: a) PTHH: Zn + H2SO4 \(\rightarrow\) ZnSO4+ H2\(\uparrow\)
b) n\(H_2SO_4\) = \(\frac{49}{98}=0,5\left(mol\right)\)
Ta có tỉ lệ: \(\frac{n_{Zn}}{1}=0,2< \frac{n_{H_2SO_4}}{1}=0,5\)
=> Zn hết, H2SO4 dư
=> Tính số mol các chất cần tìm theo Zn
Vậy sau pứ H2SO4 còn dư
c) Theo PT: n\(H_2\) = nZn = 0,2 (mol)
=> V\(H_2\) = 0,2.22,4 = 4,48 (l)
Chúc bạn thi tốt ^-^
Câu 1 :
a. Ta có PTHH :
H2SO4 + Zn -> H2 ↑ + ZnSO4
b. nH2SO4 = mH2SO4 / MH2SO4
= 49 / 98 = 0,5 mol
Ta có PTHH : H2SO4+ Zn ->H2 ↑+ZnSO4
- Trước pư : 0,5mol 0,2mol
- Trong pư : 0,2mol 0,2mol
- Sau pư : 0,3mol 0 mol
=> Zn phản ứng hết, H2SO4 còn dư ( dư 0,3 mol )
Vậy sau phản ứng H2SO4 còn dư .
c. Theo PTHH : nH2 = nZn = 0,2 mol
-> VH2SO4 ( ĐKTC ) = nH2SO4 . 22,4
= 0,2 . 22,4 = 4,48 l
Vậy sau phản ứng thu được 4,48 l .
Câu 2 :
mdd CuSO4 = Ddd CuSO4 . Vdd CuSO4
= 1,206 . 165,84 =200003,04g
-> C% = mct / mdd . 100%
= mCuSO4 / mdung dịch CuSO4 . 100%
= 36 / 200003,04 . 100%
= 0,00017999726 %
Vậy C% của dung dịch CuSO4 đã dùng là 0,00017999726 % .
Kết quả của câu 2 thì bạn nên làm tròn nha chứ không phải như thế đâu ^-^
mdd = 1,206 . 165,84 = 200 (g)
=> C%dd = \(\frac{36}{200}.100\%=18\%\)