Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

`2Fe + 6H_2 SO_[4(đ,n)] -> Fe_2(SO_4)_3 + 3SO_2 \uparrow + 6H_2 O`
`0,05` `0,15` `0,025` `(mol)`
`Cu + 2H_2 SO_[4(đ,n)] -> CuSO_4 + SO_2 \uparrow + 2H_2 O`
`0,225` `0,45` `0,225` `(mol)`
`n_[SO_2]=[6,72]/[22,4]=0,3(mol)`
Gọi `n_[Fe]=x` ; `n_[Cu]=y`
`=>` $\begin{cases} \dfrac{3}{2}x+y=0,3\\56x+64y=17,2 \end{cases}$
`<=>` $\begin{cases}x=0,05\\y=0,225 \end{cases}$
`@m_[Fe_2(SO_4)_3]=0,025.400=10(g)`
`@m_[CuSO_4]=0,225.160=36(g)`
`@m_[dd H_2 SO_4]=[(0,15+0,45).98]/80 .100=73,5(g)`
Sửa đề: 80% ---> 98% (80% chưa đặc nên không giải phóng SO2 được)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(\rightarrow56a+64b=17,2\left(1\right)\)
PTHH:
\(2Fe+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
a------>3a------------------->0,5a--------------->1,5a
\(Cu+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\)
b----->2b------------------->b------------->b
\(\rightarrow1,5a+b=\dfrac{6,72}{22,4}=0,3\left(2\right)\)
Từ \(\left(1\right)\left(2\right)\rightarrow\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,225\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe_2\left(SO_4\right)_3}=0,5.0,05.400=10\left(g\right)\\m_{CuSO_4}=0,225.160=36\left(g\right)\\m_{ddH_2SO_4}=\dfrac{\left(0,05.3+0,225.2\right).98}{98\%}=60\left(g\right)\end{matrix}\right.\)

Chọn A
Cách 1:
Giả thiết hỗn hợp ban đầu được tạo ra từ a mol Fe và b mol O 2
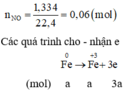

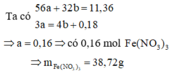
Cách 2:
Quy đổi hỗn hợp về Fe (x mol) và O (y mol)
→ 56x + 16y = 11,36 mol (1)
Bảo toàn e: 3nFe = 2nO + 3 nNO
→ 3x – 2y = 0,18 (2)
Từ (1)(2) → x = 0,16; y = 0,15
Số mol NO3- = ne cho = 3 nFe = 0,48 mol
mmuối = mFe + mNO3- = 0,16.56 + 0,48.62 = 38,72g

Gọi số mol Cu, M là a, b (mol)
=> 64a + b.MM = 11,2 (1)
\(n_{NO}=\dfrac{3,92}{22,4}=0,175\left(mol\right)\)
Cu0 - 2e --> Cu+2
a--->2a
M0 - ne --> M+n
b--->bn
N+5 + 3e --> N+2
0,525<-0,175
Bảo toàn e: 2a + bn = 0,525 (2)
(1)(2) => 32bn - bMM = 5,6 (3)
\(n_{H_2}=\dfrac{3,136}{22,4}=0,14\left(mol\right)\)
PTHH: 2M + 2xHCl --> 2MClx + xH2
\(\dfrac{0,28}{x}\)<---------------------0,14
=> \(\dfrac{0,28}{x}=b\) (4)
(3)(4) => MM = 32n - 20x (g/mol)
Và \(0< x\le n\)
TH1: x = n = 1 => MM = 12 (Loại)
TH2: x = n = 2 => MM = 24 (Mg)
TH3: x = n = 3 => MM = 36 (Loại)
TH4: x = 1; n = 2 => MM = 44 (Loại)
TH5: x = 1; n = 3 => MM = 76 (Loại)
TH6: x = 2; n = 3 => MM = 56 (Fe)
Vậy M có thể là Mg hoặc Fe
=> C

Đáp án A.
Gọi nAl = a mol, nZn = b mol.

Ta có: 27a + 65b = 9,2 (*)
3a + 2b = 0,5 (**)
Giải (*), (**): a = b = 0,1 mol.
m muối = mKl + M gốc axit. ne/2
= 3,92 + 96. 0,25 = 33,2 g

nH2=4,48/22,4=0,2 mol
Fe +2HCl -->FeCl2+H2
0,2 0,2 mol
=>mFe=0,2*56=11,2 g
nSO2=10,08/22,4=0,45 mol
gọi số mol của Cu là a mol
bảo toàn e ta có
Cu\(^0\)-->Cu\(^{+2}\)+2e
a 2a S\(^{+6}\) + 2e -->S\(^{+4}\)
Fe\(^0\)--> Fe\(^{+3}\)+3e 0,45 0,9
0,2 0,6
=>a=0,15=>mCu=0,15*64=9,6 g
=>mhh=9,6+11,2=20,8g
=>%Cu=9,6*100/20,8=46,15%





Xl bài này cân bằng pt bị sai
Câu 1:
PTHH: \(3R+8HNO_3\rightarrow3R\left(NO_3\right)_2+4H_2O+2NO\) (1)
Số mol: 0,15 (mol )-----------------------------------------> 0,1 (mol)
Theo đề: nNO = \(\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Mặt khác, theo phương trình: nR = \(\dfrac{3}{2}\) nNO = \(\dfrac{3}{2}\) . 0,1 = 0,15 (mol)
Mà: mR = 9,75 (g) \(\Rightarrow M_R=\dfrac{9,75}{0,15}=65\left(đvC\right)\)
Vậy R là kẽm (Zn).
Câu 2:
Theo đề: nhỗn hợp khí = \(\dfrac{8,96}{22,4}=0,4\left(mol\right)\).
Gọi x, y lần lượt là số mol của NO và NO2.
PTHH: \(3Cu+8HNO_3\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\left(1\right)\)
Số mol: \(\dfrac{3}{2}x\) -----------------------------------------> x
\(Cu+4HNO_3\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\left(2\right)\)
Số mol: \(\dfrac{1}{2}y\) -------------------------------------> y
Gọi x, y lần lượt là số mol của NO và NO2.
Theo đề: \(m_{NO}+m_{NO_2}=15,2\Leftrightarrow30x+46y=15,2\) (3)
Mặt khác: nhỗn hợp khí = \(n_{NO}+n_{NO_2}\Leftrightarrow x+y=0,4\left(4\right)\)
Từ (3) và (4) ta được hệ phương trình: \(\left\{{}\begin{matrix}30x+46y=15,2\\x+y=0,4\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
Theo (1) và (2): \(\sum n_{Cu}=\dfrac{3}{2}x+\dfrac{1}{2}y=\dfrac{3}{2}.0,2+\dfrac{1}{2}.0,2=0,4\left(mol\right)\)
\(\Rightarrow m=m_{Cu}=0,4.64=25,6\left(g\right)\)
Câu 3:
Đây là phản ứng oxi hóa - khử. Theo đề: \(n_{SO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Gọi x, y lần lượt là số mol của Mg và Al tham gia phản ứng.
Ta có: * Qúa trình oxi hóa:
+ \(Mg^0\rightarrow Mg^{2+}+2e\)
Số mol: x ------------------> 2x
+ \(Al^0\rightarrow Al^{3+}+3e\)
Số mol: y ----------------> 3y
* Qúa trình khử: \(S^{6+}+2e\rightarrow S^{4+}\)
Số mol: 0,2 <--- 0,1
Áp dụng định luật bảo toàn điện tích, ta có: 2x + 3y = 0,2 (mol) (1)
Mặt khác: mX = mMg + mAl hay: 24x + 27y = 0,51 (g) (2)
Từ (1) và (2) ta có hệ phương trình: ........... giải ra số âm rồi bn ơi. Hình như nhầm ở đâu đó. Sorry!
n cx lm giống mk ak?