Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
![]() = 0,8 mol
= 0,8 mol
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,8 → ![]() = 0,72 (mol)
= 0,72 (mol)
Vkhí = 0,72.22,4 = 16,128 (lit)
nNaOH = 2 (mol)
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,72 2 → 0,72 0,72 (mol)
do NaOH dư, tính theo Cl2
Dung dịch sau phản ứng: nNaCl = nNaClO = 0,72 (mol)
nNaOH dư = 0,56 (mol)
CNaCl = CNaClO = 1,44M, CNaOH = 1,12M

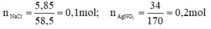
a) Phương trình hóa học của phản ứng:
NaCl + AgNO3 → AgCl↓ + NaNO3
Theo pt: nAgNO3 pư = nAgCl = nNaCl = 0,1 mol
b) Vdd = 300 + 200 = 500 ml
nAgNO3 dư = 0,2 – 0, 1 = 0,1 mol; nNaNO3 = nNaCl = 0,1 mol
CM(NaNO3) = CM(AgNO3) = 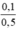 = 0,2 mol/l.
= 0,2 mol/l.

Đáp án D
nNaCl =0,1 mol, nAgNO3 = 0,2 mol
NaCl + AgNO3 → AgCl + NaNO3
0,1 → 0,1 0,1 (mol)
Vdd = 300 + 200 = 500 ml
![]() (dư) = 0,2 - 0,1 =0, 1 (mol)
(dư) = 0,2 - 0,1 =0, 1 (mol)
![]() = 0,1 mol
= 0,1 mol
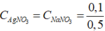 = 0,2 M
= 0,2 M

\(n_{MnO_2}=\dfrac{69,6}{87}=0,8\left(mol\right)\)
nKOH = 0,5.4 = 2(mol)
PTHH: MnO2 + 4HCl --> MnCl2 + Cl2 + 2H2O
0,8------------------------>0,8
2KOH + Cl2 --> KCl + KClO + H2O
Xét tỉ lệ \(\dfrac{2}{2}>\dfrac{0,8}{1}\) => KOH dư, Cl2 hết
2KOH + Cl2 --> KCl + KClO + H2O
1,6<--0,8---->0,8---->0,8
=> \(\left\{{}\begin{matrix}n_{KOH\left(dư\right)}=2-1,6=0,4\left(mol\right)\\n_{KCl}=0,8\left(mol\right)\\n_{KClO}=0,8\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(KOH\right)}=\dfrac{0,4}{0,5}=0,8M\\C_{M\left(KCl\right)}=\dfrac{0,8}{0,5}=1,6M\\C_{M\left(KClO\right)}=\dfrac{0,8}{0,5}=1,6M\end{matrix}\right.\)

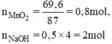
a) Phương trình hóa học của phản ứng:
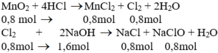
b) Theo pt (1): nCl2 = nMnCl2 = nMnO2 = 0,8 mol
Theo pt (2): nNaCl = nNaClO = nCl2 = 0,8 mol
nNaOH pư = 2. nCl2 = 2. 0,8 = 1,6 mol
⇒ nNaOH dư = 2 - 1,6 = 0,4 mol
Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM (NaCl) = CM (NaClO) = CM(MnCl2) = 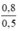 = 1,6 mol/ lit
= 1,6 mol/ lit
CM (NaOH)dư = 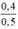 = 0,8 mol/ lit
= 0,8 mol/ lit

\(a.n_{CaCl_2}=0,1\left(mol\right)\\ CaCl_2+2AgNO_3\rightarrow Ca\left(NO_3\right)_2+2AgCl\\ n_{AgCl}=2n_{CaCl_2}=0,2\left(mol\right)\\ \Rightarrow m_{AgCl}=0,2.143,5=28,7\left(g\right)\\ b.n_{Ca\left(NO_3\right)_2}=n_{CaCl_2}=0,1\left(mol\right)\\ \Rightarrow CM_{CaCl_2}=\dfrac{0,1}{0,1}=1M\)



1)
nNaOH = 0,5 x 4 = 2 mol
a) Phương trình hóa học của phản ứng :
MnO2 + 4 HCl → MnCl2 + Cl2 +2H2O
0,8 mol 0,8mol 0,8 mol
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,8 mol → 1,6 mol. 0,8mol 0,8mol
b) Nồng độ mol/l của các chất trong dung dịch sau phản ứng:
CM(NaCl) = CM(MnCl2) = CM(NaClO) = 0,8 /0,5 = 1,6 mol/l
CM(NaOH)dư = (2. 1,6)/0,5 = 0,8 mol/l
câu 3
nNaCl =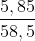 = 0,1 mol;
= 0,1 mol; 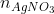 =
= 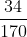 = 0,2 mol
= 0,2 mol
a) Phương trình hóa học của phản ứng:
NaCl + AgNO3 → AgCl↓ + NaNO3
0,1 mol 0,1 mol 0,1 mol 0,1 mol
mAgCl = 143,5 x 0,1 = 14,35g
b) Vdd = 300 + 200 = 500 ml
Câu 1 ( Tính m nha Linh )
Câu 1:
\(n_{KMnO4}=\frac{9,48}{39+55+16.4}=0,06\left(mol\right)\)
\(2KMnO_4+16HCl\rightarrow2MnCl_2+5Cl_2+2KCl+8H_2O\)
\(\Rightarrow n_{KMnO4_{pư}}=0,0.80\%=0,048\left(mol\right)\)
\(\Rightarrow n_{Cl2}=\frac{5}{2}n_{KMnO4_{pư}}=0,12\left(mol\right)\)
\(2Fe+3Cl_2\rightarrow2FeCl_3\)
\(n_{Fe}=\frac{5,6}{56}=0,1\left(mol\right)>\frac{2}{3}n_{Cl2}\) nên Fe dư.
BTKL, \(m=m_{Fe}+m_{Cl2}=5,6+0,12.\left(35,5.2\right)=14,12\left(g\right)\)
Câu 2 :
\(MnO_2+4HCl\rightarrow MnCl_2+Cl_2+2H_2O\)
\(n_{MnO2}=\frac{69,6}{55+16.2}=0,8\left(mol\right)\)
Theo PT: \(n_{Cl2}=n_{MnO2}=0,8\left(mol\right)\)
\(n_{NaOH}=0,5.4=2\left(mol\right)\)
Cho Cl2 vào dung dịch NaOH
\(2NaOH+Cl_2\rightarrow NaCl+NaClO+H_2O\)
Vì nNaOH > 2nCl2 nên NaOH dư
\(\Rightarrow n_{NaOH_{pư}}=2n_{Cl2}=0,8.2=1,6\left(mol\right)\Rightarrow n_{NaOH_{Dư}}=2-1,6=0,4\left(mol\right)\)
\(n_{NaCl}=n_{NaClO}=n_{Cl2}=0,8\left(mol\right)\)
\(\Rightarrow CM_{NaOH_{Dư}}=\frac{0,4}{0,5}=0,8M\)
\(\Rightarrow CM_{NaCl}=CM_{NaClO}=\frac{0,8}{0,5}=1,6M\)