Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
Phản ứng phân hủy
b) \(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
PTHH: 2KNO3 --to--> 2KNO2 + O2
0,15<--------------------0,075
=> \(m_{KNO_3\left(PTHH\right)}=0,15.101=15,15\left(g\right)\)
=> mKNO3 (thực tế) = \(\dfrac{15,15.100}{85}=17,824\left(g\right)\)
c) \(n_{KNO_3\left(pư\right)}=\dfrac{10,1.80\%}{101}=0,08\left(mol\right)\)
=> nO2 = 0,04 (mol)
=> VO2 = 0,04.22,4 = 0,896(l)

a) PTHH:
2KNO3→2KNO2 + O2
b)\(n_{O_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)Theo PTHH ta có:
nKNO3=2nO2=0,15(mol)
mKNO3 ban đầu=0,15.101=15,15(g)
mKNO3 thực tế=15,15.\(\dfrac{85}{100}\)=12,8775(g)

a.
KN03 --> KN02 + 1/2 02
b.
n 02 = 0,075 mol
mà H% đạt 85%
=> n 02 lí thuyết thu đc = 0,075*100/85 = 3/34 mol
KN03 --> KN02 + 1/2 02
3/17 mol <---- 3/34 mol
vậy n KN03 = 3/17 mol
c.
n KN03 = 0,1
KN03 ---> KN02 + 1/2 02
lí thuyết:..0,1 -----------------> 0,05
mà H% = 80%
=> n 02 thu được = 0,05*80/100 = 0,04 mol
=> V 02 thực tế thu dc = 0,896 lit

Câu 6.
\(n_{O_2}=\dfrac{16,8}{22,4}=0,75mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
1,5 0,75
\(m_{KMnO_4}=1,5\cdot158=237g\)
Câu 7.
\(n_{Fe_3O_4}=\dfrac{4,64}{232}=0,02mol\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
0,04 0,02
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{2}{75}\) 0,04
\(m_{KClO_3}=\dfrac{2}{75}\cdot122,5=\dfrac{49}{15}\approx3,27g\)

Bài 1.
\(n_{Mg}=\dfrac{2,4}{24}=0,1mol\)
\(2Mg+O_2\underrightarrow{t^o}2MgO\)
Đây là phản ứng hóa hợp vì chất sản phẩm được tạo từ 2 chất ban đầu.
\(n_{O_2}=2n_{Mg}=0,2mol\)
\(V=0,2\cdot22,4=4,48\left(l\right)\)
Bài 2.
\(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
\(n_{O_2}=\dfrac{1,68}{22,4}=0,075mol\)
\(n_{KNO_3}=2n_{O_2}=0,15mol\)\(\Rightarrow m_{KNO_3}=0,15\cdot101=15,15g\)

Bạn tách ra từng câu nhé!
Bài 3.
\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{36}{56}=0,6428mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
0,6428 ----- 0,4285 ( mol )
\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
0,857 0,4285 ( mol )
\(m_{KMnO_4}=n_{KMnO_4}.M_{KMnO_4}=0,857.158=135,406g\)
Bài 4.
a.\(n_{Al_2O_3}=\dfrac{m_{Al_2O_3}}{M_{Al_2O_3}}=\dfrac{51}{102}=0,5mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
1 0,75 0,5 ( mol )
\(m_{Al}=n_{Al}.M_{Al}=1.27=27g\)
\(V_{O_2}=n_{O_2}.22,4=0,75.22,4=16,8l\)
b.\(2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\)
1,5 0,75 ( mol )
\(m_{KMnO_4}=n_{KMnO_4}.M_{KMnO_4}=1,5.158=237g\)
\(2KClO_3\rightarrow\left(t^o\right)2KCl+3O_2\)
0,5 0,75 ( mol )
\(m_{KClO_3}=n_{KClO_3}.M_{KClO_3}=0,5.122,5=61,25g\)

\(PTHH:2KNO_3\overset{t^0}{\rightarrow}2KNO_2+O_2\)
\(a,n_{O_2}=\frac{11,2}{32}=0,35mol\)
\(\Rightarrow n_{KNO_3}=\frac{0,35}{80}.101=44,1875g\)
\(b,n_{KNO_3}=\frac{40,4}{101}=0,4mol\)
\(\Rightarrow m_{O_2}=0,4.32.85\%=10,88g\)
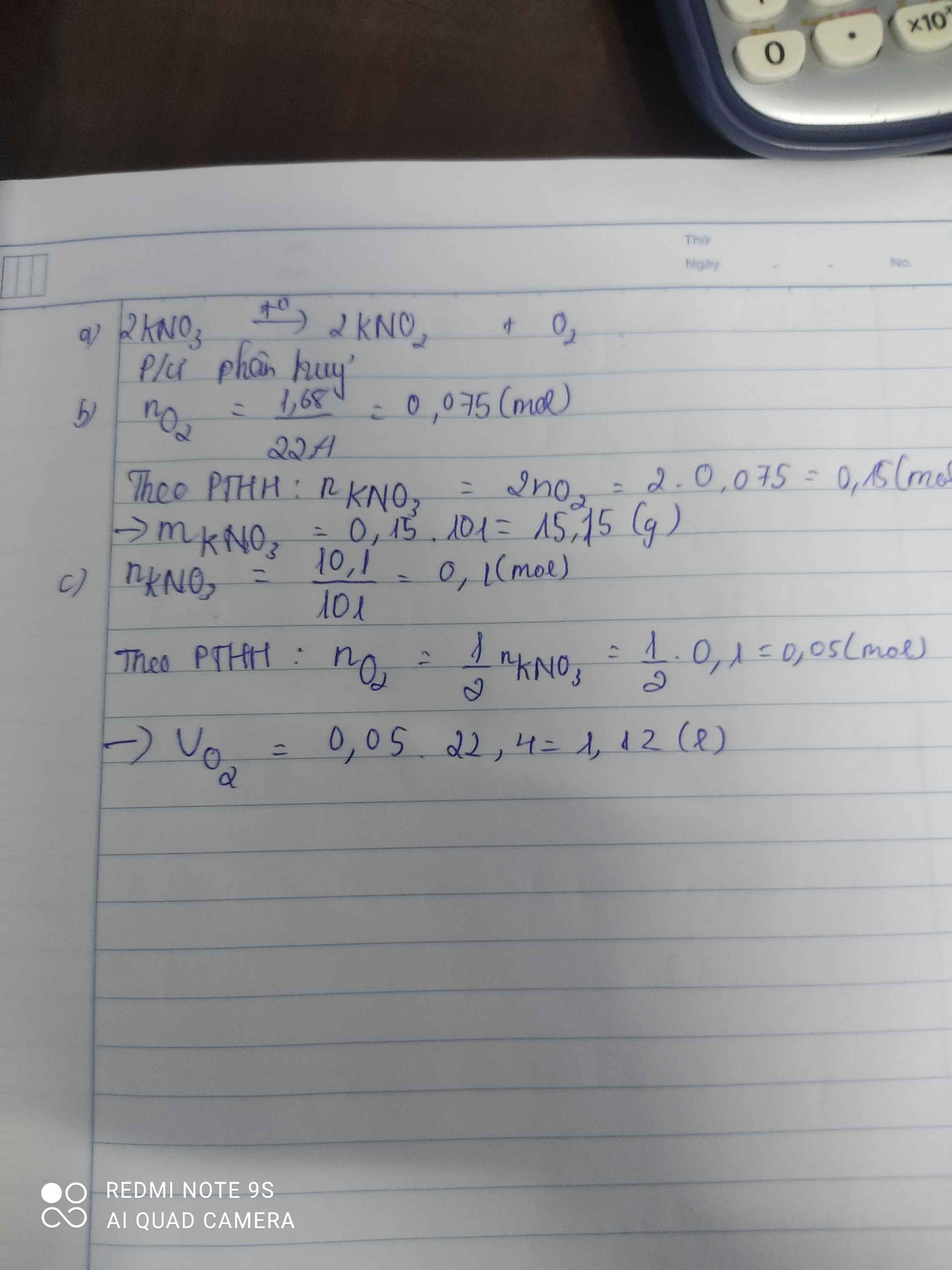





Bài 1
2KClO3--->2KCl+3O2
Theo pthh
n O2=3/2n KClO3=0,75(mol)
m O2=0,75.32=24(g)
Bài 2
a)2KNO3-->2KNO2+O2
b)n O2=1,68/22,4=0,075(mol)
Theo pthh
n KNO3=2n O2=0,15(mol)
m KNO3=0,15.101=15,15(g)
H=85%
-->m KNO3=12,8775(g)
Bài 3
2KClO3--->2KCl+3O2
2O2+CH4--->CO2+2H2O
O2+2H2--->2H2O
Theo pthh2
n O2=2n CH4=1(mol)
Theo pthh3
n O2=1/2n H2=0,125(mol)
\(\sum n_{O2}\) cần =0,125+1=1,125(mol)
Theo pthh1
n KClO3=2/3 n O2=0,75(mol)
m KClO3=0,75.122,5=91,875(g)
Bài 3
bai 2 b đáp án là 17,82 ms đúng thì phải cj ơi..
Sao tới 2 cái bài 3 lận vậy cj? mà cái "Bài 3" đầu tiên nó ko giống đề. Dường như có lỗi... Bài 1 thì giống cách em luôn!
tth_new cái bài 3 sau là lỗi ý
Bài 2 cj thấy đúng mà nhỉ
mà bài 2 làm sao tính được lượng KNO3 ở cuối bài cj vậy ạ?
Bài 1 :
\(PTHH:2KClO_3\rightarrow2KCl+3O_2\)
_________0,5_______________0,5
\(\rightarrow m_{O2}=0,75.32=24\left(g\right)\)
Bài 2 :
\(a,PTHH:2KNO3\rightarrow2KNO_2+O_2\)
Ta có : \(n_{O2}=\frac{1,68}{22,4}=0,075\left(mol\right)\)
\(b,\)
nKNO3 theo phương trình là \(0,075.2=0,15\left(mol\right)\)
\(\rightarrow n_{KNO3_{tt}}=\frac{0,15}{85\%}=\frac{3}{17}\left(mol\right)\)
\(\rightarrow m_{KNO3}=\frac{101.3}{17}=17,82\left(g\right)\)
Bài 3:
\(PTHH:CH_4+5O_2\rightarrow4CO2+2H_2O\)
\(2H_2+O_2\rightarrow2H_2O\)
Ta có : \(n_{O2\left(1\right)}=5.nCH_4=5.0,5=2,5\left(mol\right)\)
\(n_{O2\left(2\right)}=\frac{1}{2}nH_2=0,125\left(mol\right)\)
Tổng số mol O2: nO2=2,625 (mol)
\(2KClO_3\rightarrow2KCl+3O_2\)
\(n_{KClO_3}=\frac{2}{3}nO_2=1,75\left(mol\right)\)
\(\rightarrow m_{KClO_3}=1,75.22,4=214,375\left(g\right)\)
Duong Le cái bài 3 đầu tiên em thấy nó sao sao ..
Chỗ dấu -> ở giữa bài 2 b em ko hiểu cho lắm.
tth_new bài 2 vì hiệu suất =85% nên lấy 15,15.85/100=12,8775
Tính số mol của KNO3 thực tế
Bài 3 phương trình đầu là bỏ 5 ở O2 đi nhé viết lộn
Nên sửa lại toàn bài hộ cj nhé nếu không được thì cj sẽ trả lời lại tth_new
buithianhtho như sao lại chia 85% á cj? em tưởng là 0,15 . 85/100
buithianhtho chị tl luôn đi, em sửa hay lộn lắm..
Viết tắt e thích viết kiểu nào cũng được
buithianhtho bài 3 cân bằng pt 1 sai sao ý
\(CH_4+2O_2\rightarrow CO_2+2H_2O\)
\(2H_2+O_2\rightarrow2H_2O\)
Ta có : \(n_{O2\left(1\right)}=2.n_{CH4}=2.0,5=1\left(mol\right)\)
\(n_{O2\left(2\right)}=\frac{1}{2}n_{H2}=0,125\left(mol\right)\)
Tổng số mol O2: nO2=1,125 (mol)
\(2KClO_3\rightarrow2KCl+3O_2\)
\(n_{KClO_3}=\frac{2}{3}n_{O2}=0,75\left(mol\right)\)
\(\rightarrow m_{KClO3}=0,75.122,5=91,875\left(g\right)\)
Duong Le thì t nói rồi mà
Duong Lebuithianhtho cj giúp em bài này luôn nha:Câu hỏi của tth_new - Hóa học lớp 8 | Học trực tuyến
nO2(1) là sao ạ?
2 phương trình đó emtth_new