Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu hỏi của Dịch Thiên Tổng - Hóa học lớp 8 | Học trực tuyến

nFe = \(\frac{11,2}{56}=0,2mol\)
nAl = \(\frac{m}{27}mol\)
Cốc A : Fe + 2HCl -> FeCl2 + H2
0,2 0,2
Theo định luật bảo toàn khối lượng khối lượng HCl tăng thêm;
11,2 - 0,2.2 = 10,8 g
Cốc B : 2Al + 3H2SO4 -> Al2(SO4)3 + 2H2
\(\frac{m}{27}\) \(\frac{3m}{27.2}\)
Khi cho mg Al vào cốc B thì cốc B tăng thêm là ;
m - \(\frac{3m}{27.2}\).2 = 10,8
=> m = 12,15 g

Cốc A: Fe + 2HCl ---> FeCl2 + H2 (1)
0,2 0,2 mol
Cốc B: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2 (2)
m/27 m/18 mol
Số mol Fe = 11,2/56 = 0,2 mol; số mol Al = m/27 mol.
Khối lượng cốc A tăng = khối lượng Fe - khối lượng H2 (bay ra) = 11,2 - 2.0,2 = 10,8 gam.
Khối lượng cốc B tăng = khối lượng Al - khối lượng H2 = m - 2.m/18 = m - m/9 = 8m/9 gam.
Vì cân ở vị trí cân bằng nên khối lượng tăng cốc A = khối lượng tăng ở cốc B. Suy ra: 8m/9 = 10,8 hay m = 12,15 g
Cốc A: Fe + 2HCl ---> FeCl2 + H2 (1)
0,2 0,2 mol
Cốc B: 2Al + 3H2SO4 ---> Al2(SO4)3 + 3H2 (2)
m/27 m/18 mol
Số mol Fe = 11,2/56 = 0,2 mol; số mol Al = m/27 mol.
Khối lượng cốc A tăng = khối lượng Fe - khối lượng H2 (bay ra) = 11,2 - 2.0,2 = 10,8 gam.
Khối lượng cốc B tăng = khối lượng Al - khối lượng H2 = m - 2.m/18 = m - m/9 = 8m/9 gam.
Vì cân ở vị trí cân bằng nên khối lượng tăng cốc A = khối lượng tăng ở cốc B. Suy ra: 8m/9 = 10,8 hay m = 12,15 g

\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 0,2
\(\Rightarrow m_{Fe}+m_{H_2SO_4}=0,2\cdot56+0,2\cdot98=30,8g\)
Cả hai đĩa cân thăng bằng:
\(m_{Fe}+m_{H_2SO_4}=m_{Al}+m_{H_2SO_4}\)
\(\Rightarrow m_{Fe}=m_{Al}=11,2g\)

\(Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = n_{Fe} = \dfrac{11,2}{56} =0,2(mol)\\ \Rightarrow m_{tăng} = 11,2 - 0,2.2 = 10,8(gam)\\ 2Al +3 H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ n_{Al} = \dfrac{m}{27}(mol)\\ \Rightarrow n_{H_2} = \dfrac{3}{2}n_{Al} = \dfrac{m}{18}(mol)\)
Vì cân ở vị trí thăng bằng nên :
\(m - \dfrac{m}{18}.2 = 10,8\Rightarrow m =12,15(gam)\)

Fe + 2HCl → FeCl2 + H2
Theo PTHH :
n H2 = n Fe = 11,2/56 = 0,2(mol)
=> m tăng = m Fe - m H2 = 11,2 - 0,2.2 = 10,8(gam)
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
n Al = m/27
n H2 = 3/2 n Al = m/18(mol)
=> m tăng = m Al - m H2 = m - m/18 . 2 = 8m/9(gam)
Vì cân thăng bằng nên : 10,8 = 8m/9
=> m = 12,15 (gam)

Em ơi đề hơi kì nha, cốc A đựng dd HCl, cốc B đựng dd H2SO4 vậy cốc ở đâu đựng nước?
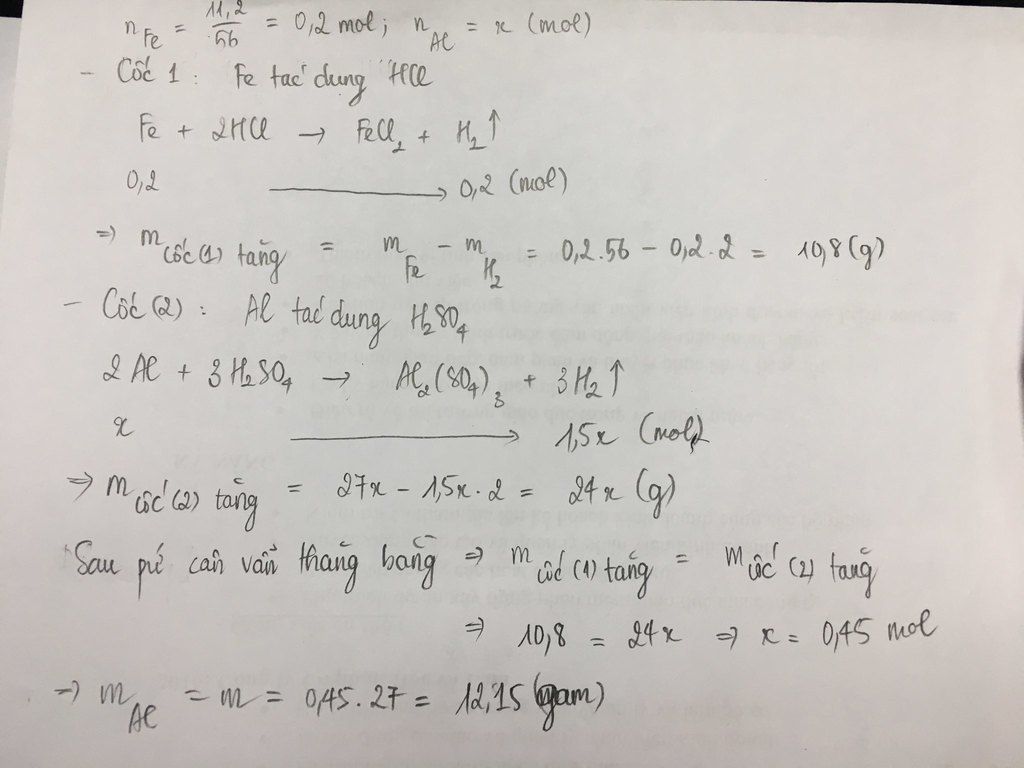

giúp tôi với
mai nộp cô
1 .
\(nFe=11,2\div56=0,2\left(mol\right)\)
\(nAi=\frac{m}{27}\)\(\left(mol\right)\)
Khi them Fe vao coc dung dd HCl ( coc A ) co phan ung :
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Theo dinh luat bao toan nang luong , khoi luong coc dung HCl tang them :
\(2Al+3H_2SO_4\Rightarrow Al_2\left(SO_4\right)_3+3H_2\)
- Khi cho m gam vao Al vao coc B , coc B tang them m \(\frac{3.m}{27.2}\)
- De can thang bang khoi luong o coc dung H2SO4 , cung phai tang them 10,8 g . co
\(m=12,15\left(g\right)\)
2 .
a) Hiện tượng pứ: CuO đen sau pứ thành đỏ và có hơi nước bốc lên
b) Pt: CuO + H2 --to--> Cu + H2O
........1 mol...................1 mol
..........x..........x.................x
nCuO ban đầu = \(\dfrac{20}{80}=0,25\) mol
Nếu CuO pứ hết => nCu = 0,25 mol
=> mCu = 0,25 .64 = 16g < 16,8g
Vậy CuO không pứ hết
Gọi x là số mol của CuO pứ
Ta có: mCuO dư + mCu = mchất rắn
\(\Leftrightarrow\left(0,25-x\right)80+64x=16,8\)
\(\Leftrightarrow x=0,2\) mol
Hiệu suất pứ:
H = \(\dfrac{0,2}{0,25}.100\%=80\%\)
c) nH2 = nCuO pứ = 0,2 mol
=> VH2 = 0,2 . 22,4 = 4,48 (lít)
3 .
H2 + CuO ---> Cu + H2O
x x x
a) xuất hiện các tinh thể đồng (màu đồng) trong ống nghiệm và có hơi nước bám trên thành ống nghiệm.
b) Số mol CuO ban đầu = 20/80 = 0,25 mol. Gọi x là số mol CuO đã tham gia phản ứng. Số mol CuO còn dư = 0,25 - x mol. Số mol Cu là x mol.
Khối lượng chất rắn sau phản ứng = khối lượng CuO dư + khối lượng Cu = 80(0,25-x) + 64x = 16,8. Thu được x = 0,2 mol.
Số mol H2 = x = 0,2 mol. Nên V = 0,2.22,4 = 4,48 lít.
4 .
H2 + CuO ---> Cu + H2O
x x x
a) xuất hiện các tinh thể đồng (màu đồng) trong ống nghiệm và có hơi nước bám trên thành ống nghiệm.
b) Số mol CuO ban đầu = 20/80 = 0,25 mol. Gọi x là số mol CuO đã tham gia phản ứng. Số mol CuO còn dư = 0,25 - x mol. Số mol Cu là x mol.
Khối lượng chất rắn sau phản ứng = khối lượng CuO dư + khối lượng Cu = 80(0,25-x) + 64x = 16,8. Thu được x = 0,2 mol.
Số mol H2 = x = 0,2 mol. Nên V = 0,2.22,4 = 4,48 lít.
5 .
Gọi thể tích dung dịch HCl 18,25% là a(ml)
⇒mdung dịch HCl=1,2.a(gam)⇒mdung dịch HCl=1,2.a(gam)
⇒nHCl=1,2a.18,25%36,5=0,006a(mol)⇒nHCl=1,2a.18,25%36,5=0,006a(mol)
Gọi thể tích dung dịch HCl 13% là b(ml)$
⇒mdung dịch HCl=1,123b(mol)⇒mdung dịch HCl=1,123b(mol)
⇒nHCl=1,123b.13%36,5=0,004b(mol)⇒nHCl=1,123b.13%36,5=0,004b(mol)
Sau phản ứng, Vdd=a+b(ml)=0,001a+0,001b(lít)Vdd=a+b(ml)=0,001a+0,001b(lít)
⇒CMHCl=0,006a+0,004b0,001a+0,001b=4,5M⇒CMHCl=0,006a+0,004b0,001a+0,001b=4,5M
⇒ab=13
thank