Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Các chất điện li mạnh phân li hoàn toàn nên phương trình điện li và nồng độ các ion trong dung dịch như sau:
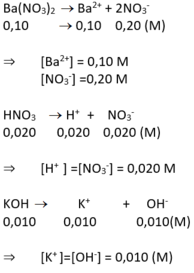
Ba(NO3)2 → Ba2+ + 2NO-3
0,01M 0,10M 0,20M
HNO3 → H+ + NO-3
0,020M 0,020M 0,020M
KOH → K+ + OH-
0,010M 0,010M 0,010M
b) Các chất điện li yếu phân li không hoàn toàn nên phương trình điện li như sau:
HClO H+ + ClO-
HNO2 H+ + NO-2.

Đáp án D.
Do khi hoà tan (trong nước) các phân tử chất điện li phân li ra thành các cation và anion.

a) Các chất điện li mạnh phân li hoàn toàn nên phương trình điện li và nồng độ các ion trong dung dịch như sau:
Ba(NO3)2 \(\rightarrow\) Ba2+ + 2NO-3
0,01M 0,10M 0,20M
HNO3 \(\rightarrow\) H+ + NO-3
0,020M 0,020M 0,020M
KOH \(\rightarrow\) K+ + OH-
0,010M 0,010M 0,010M
b) Các chất điện li yếu phân li không hoàn toàn nên phương trình điện li như sau:
HClO H+ + ClO-
HNO2 H+ + NO-2.

Đáp án D
(a)Đúng
(b)Sai vì HF là chất điện li yếu
(c) Sai vì đây là không là các chất điện li
(d)Sai vì có những chất tan trong nước cho dung dịch dẫn điện nhưng không gọi là chất điện li (Ví dụ SO3, CaO,…)

Đáp án C. Vì chỉ rõ các ion nào đã tác dụng với nhau làm cho phản ứng xảy ra.

- Sự điện li là sự phân li thành các cation (ion dương) và anion (ion âm) của phân tử chất điện li khi tan trong nước.
- Chất điện li là những chất tan trong nước và tạo thành dung dịch dẫn được điện.
- Các chất là chất điện li như axit, các bazơ, các muối tan được trong nước.
- Chất điện li mạnh là những chất khi tan trong nước các phân tử hoà tan đều phân li ra ion.
- Thí dụ:
H2SO4 → 2H+ + SO42-
KOH → K+ + OH-
Na2SO4 → 2Na+ + SO42-
- Chất điện li yếu là những chất khi tan trong nước chỉ có một phần số phân tử hoà tan phân li ra ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch.
- Thí dụ: H2S ⇌ H+ + HS-
Bài 7:
Chọn C.
Một hợp chất có khả năng phân li ra cation H+ trong nước là axit.
Bài 8:
Chọn D: [H+] < 0,10M.
Bài 9:
Chọn A. [H+] = 0.10M.
Bài 13:
Chọn C
Ta có: [H+] = 10-14/ 1,5. 10-5 =6,6.10-10M<10-7M ⇒môi trường kiềm
Bài 15:
Chọn B. Tích số ion của nước là hằng số ở nhiệt độ xác định
Bài 5:
Chọn A.
KCl rắn tồn tại dưới dạng tinh thể ion. Mạng tinh thể KCl tương tựu mạng tinh thể NaCl . Tinh thể ion rất bền vững vì lực hút tĩnh điện giữa các ion ngược dấu trong tinh thể ion rất lớn. Các ion K+ và Cl– chỉ dao động tại các đầu nút của mạng tinh thể (không chuyển dịch tự do) vì vậy, KCl rắn, khan không dẫn điện.
Bài 1 :
Các dung dịch HCl, NaOH, NaCl dẫn điện được vì trong dung dịch có sự hiện diện của các ion. Các dung dịch ancol etylic, saccarozơ, glixerol không dẫn điện được vì trong dung dịch không có sự hiện diện của các ion.
Bài 10:
Tích nồng độ ion H+ và nồng độ ion OH– trong nước gọi là tích số ion của nước. Ở 25°c, tích số này có giá trị 10-14
Bài 11:
Môi trường axit là môi trường trong đó [H+] > [OH–] hay [H+] > 10-7M hay pH < 7
Môi trường bazơ là môi trường trong đó [H+] < [OH–] hay [H+] < 10-7M hay pH > 7
Môi trường trung tính là môi trường trong đó [H+] = [OH–] hay [H+] = 10-7 M hay pH = 7
Bài 2 :
Quá trình phân li các chất trong nước ra ion gọi là sự điện li.
Những chất tan trong nước phân li ra ion gọi là những chất điện li
Axit, bazơ, muối là những chất điện li.
Chất điện li mạnh là các chất khi tan trong nước, các phân tử hòa tan đều phân li ra ion. Ví dụ: NH4Cl -> NH4+ + Cl–
Chất điện li yếu là chất khi tan trong nước, các phân tử hòa tan chỉ phân li một phần ra ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch. Ví dụ CH3COOH ⇔ CH3COO– + H+
Chất chỉ thị axit – bazơ là chất có màu biến đổi phụ thuộc vào giá trị pH của dung dịch
Bài 3. ( mk chép mạng ko biết có giúp gì cho bạn được ko )
a) Các chất điện li mạnh phân li hoàn toàn nên phương trình điện li và nồng độ các ion trong dung dịch như sau:
Ba(NO3)2 → Ba2+ + 2NO–3
0,01M 0,10M 0,20M
HNO3 → H+ + NO–3
0,020M 0,020M 0,020M
KOH → K+ + OH-
0,010M 0,010M 0,010M
b) Các chất điện li yếu phân li không hoàn toàn nên phương trình điện li như sau:
HClO ⇔ H+ + ClO–
HNO2 ⇔ H+ + NO–2.
Bài 6:
a) H2S ⇔ H+ + HS– ;
HS– ⇔ H+ + S2–
H2CO3 ⇔ H+ + HCO3– ;
HCO3– ⇔ H + + CO32-
b) LiOH → Li+ + OH–
c) K2CO3 → 2K+ + CO32- ;
NaClO → Na+ + CIO–
NaHS → Na+ + HS–:
HS– ⇔ H+ + S2-
d) Sn(OH)2 ⇔ Sn2++ 2OH–;
H2SnO2 ⇔ 2H+ + SnO22-.
Bài 14:(mk chép mạng ko biết có giúp gì cho bạn được ko )
Dung dịch HCl 0,1M: HC1 → H+ + Cl–
0,1M 0,1M
⇒[H+] = 0,1M ⇒ [OH–]= 10-14/0,1 =10-13M ⇒ pH = -lg 0,1 = 1
Dung dịch NaOH: NaOH → Na+ + OH–
0,01M 0,01M
⇒[OH–] = 0,01M ⇒ [H+] = 10-14/0,01 =10-12M ⇒ pH = – lg 10-12 = 12
Dài quá !


Nhìn hoa hết cả mắt
Mk làm từng câu 1 nha
Bài 4 :
Chọn D.
Dung dịch chất điện li dẫn điện được do sự chuyển dịch của cả cation và anion.