Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: P = E = 26 hạt
<=> 2p = 52 hạt ( p = e)
Mặt khác: N = (2p - 22)
<=> 52 - 22 = 32 hạt
Vậy Proton = electron = 26
Nơtron = 32 hạt

a. Nguyên tử X:
\(\left\{{}\begin{matrix}2P+N=52\\2P-N=16\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=17=E=Z\\N=18\end{matrix}\right.\)
Sơ đồ đơn giản:
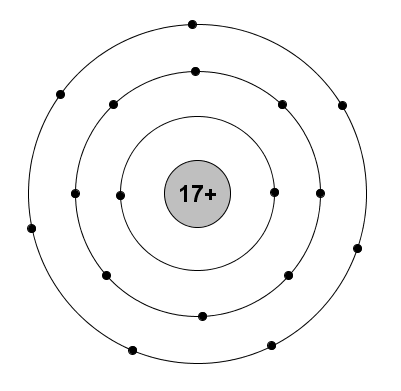
b. * Nguyên tử Y:
\(\left\{{}\begin{matrix}2P+N=28\\N\approx35,7\%.28=10\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=Z=9\\N=10\end{matrix}\right.\)
Sơ đồ cấu tạo nguyên tử Y:
Em tham khảo nha!

Tổng số hạt bằng 34 , ta có : p + n + 3 = 34 (1)
Số hạt mang điện nhiều hơn số hạt không mang điện là 10 ta có:
p + e - n = 10 (2)
mà số p = số e (3)
Từ (1), (2), (3) ta có: p = e = 11; n = 12
Chúc bạn học tốt ![]()
Ta có :
p + n + e = 34 => 2p + n = 34 (1)
mà : 2p - n = 10 (2)
TỪ 1 và 2 => 2p = 22 => p = 11 (hạt )
=> e = 11 (hạt )
=> n = 12 (hạt)

Đặt tổng số hạt p, n, e của A và B lần lượt là p, n, e
`=>` \(\left\{{}\begin{matrix}p+e+n=78\\p+e-n=26\\p=e\end{matrix}\right.\Leftrightarrow p=e=n=26\)
`=>` \(\left\{{}\begin{matrix}p_A+p_B=26\\2p_A-2p_B=28\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}p_A=20\\p_B=6\end{matrix}\right.\)
Vậy A là Canxi (Ca); B là Cacbon (C)

4, a, khối lượng cua 1 nguyen tu Pb la:
207.1,66.10-24= 34,362.10-23 g
b, khối lượng cua 39 nguyen tu Cu la:
39.64.1,66.10-24 = 41,4336.10-22 g
5,a, \(M_A=\dfrac{7,719.10^{-22}}{15.1,66.10^{-24}}=31\)
=> A la P
b, \(M_A=\dfrac{2,13642.10^{-21}}{33.1,66.10^{-24}}=39\)
=> A la K

Gọi tổng số hạt proton , electron , notron của 2 nguyên tử X và Y là M
gọi số proton , electron , notron của M lần lượt là p ,e ,n . TA CÓ :
p+e+n = 76 => 2p + n = 76 ( vì nguyên tử trung hòa về điện) (1)
do tổng số hạt mang điện tích lớn hơn tổng số hạt không mang điện tích là 24 hạt
=> 2p - n = 24
Kết hợp (1) ta được 2p = 50 => tổng số hạt mang điện tích của 2 nguyên tử X và Y là 50 hạt (*)
Từ đề ra ta lại có :
số hạt mang điện(Y) - số hạt mang điện(X) = 18(**)
Từ (*) và (**) => số hạt mang điện của Y = 34 (hạt) => Y có 17 proton => Y là nguyên tố Clo
=> số hạt mang điện của X = 16 (hạt) => X có 8 proton => X là nguyên tố Oxi

Do nguyên tử X có tổng số hạt trong nguyên tử là 40
=> 2pX + nX = 40 (1)
Do nguyên tử X có số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt
=> 2pX - nX = 12 (2)
(1)(2) => \(\left\{{}\begin{matrix}e_X=p_X=13\\n_X=14\end{matrix}\right.\) => X là Al
Nguyên tử X có số hạt mang điện là 13 + 13 = 26 (hạt)
=> Nguyên tử Y có số hạt mang điện là 26 + 8 = 34 (hạt)
=> eY = pY = 17 (hạt)
=> Y là Cl
CTHH hợp chất 2 nguyên tố X, Y có dạng AlxCly
Có: \(Al^{III}_xCl^I_y\)
=> Theo quy tắc hóa trị, ta có: x.III = y.I
=> \(\dfrac{x}{y}=\dfrac{I}{III}=\dfrac{1}{3}\)
=> CTHH: AlCl3
ta có : số hạt mạng điện tích ở X nhiều hơn số hạt ko mạng điện tích là 12
=> p+e-n = 12
<=> 2p-n=12 (p=e)
<=> n = 2p - 12 (1)
mà tổng số hạt ở X là 40
=> 2p+n=40 (2)
thay (1)vào (2) ta đc
2p+2p-12 = 40
<=> 4p = 52
<=> p = 13
=> X là nhôm : Al

\(\left\{{}\begin{matrix}2p_X+n_X=116\\2p_X-n_X=24\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}e_X=p_X=35\\n_X=46\end{matrix}\right.\)



1> ta có số p=e=26 mà số hạt mang điên nhiều hơn số hạt k mang điện là 22=> p+e-n=22=> 2p-n=22=> n=30 => A=số khối= 30+26=56
2> ta có 2p+n=28
n/ (n+p+e)=35/100<=> n/(2p+n)=0,35=> n/28=0,35=>n=10 => 2P+10=28=> p=e=9
kl: số p=số e=9 ; số n=10
vì số hạt mang điện > gấp đôi số hạt k mang điện => p+e-n=p=e=> số p=e=n
mà p+e+n=48=> p=e=n=16 => A=p+n=16+16=32
Lưu ý , lần sau nên tách thành nhiều lần hỏi , đưa 1 lần 4 câu => người ta nhìn vào đã ngại xem rồi
=====================
Bài 1 :
Theo bài ra , ta có : điện tích hạt nhân là 26+ hay p=26+ => p=e=26
Số hạt mang điện nhiều hơn số hạt không mang điện là 22
=> p + e - n=22
<=> 2p -n = 22
<=>n=30
MFe = n + p = 30 +26 =56 (đvC)
Bài 2 :
Theo bài ra : n-p=1(hạt) (I)
số hạt mang điện nhiều hơn số hạt không mang điện là 10 hạt hay : p+e-n=10 (hạt)
<=> 2p-n=10 ( hạt)
<=> -n+2p=10 (hạt) (II)
Từ (I) và (II) ta có hệ
\(\left\{{}\begin{matrix}n-p=1\\-n+2p=10\end{matrix}\right.\left\{{}\begin{matrix}n=12\left(hạt\right)\\p=11\left(hạt\right)\end{matrix}\right.\)
Vậy n=12(hạt) , p=e=11(hạt)
Bài 3 :
Theo bài ra : n+p+e=28 (hạt) <=>2p+n=28 *)
Tổng số hạt không mang điện là : n= 28.35% \(\approx10\left(hạt\right)\), thay vào (*) ta suy ra :
2p+10=28 (hạt) => p=9(hạt)
Vậy p=e=9 (hạt)
n=10 (hạt)
Bài 3 :
Ta có :
p + e + n = 28
Mà e = p => 2p + n = 28 (1)
Vì trong đó số hạt không mang điện chỉ xấp xỉ 35% nên => n = \(\dfrac{28.35}{100}=9,8\approx10\left(h\text{ạt}\right)\) Vì chỉ xấp xỉ 35%
Thay n = 10 vào (1) ta được :
2p + 10 =28 => p = e= 9 (hạt)
Vậy....
Bài 4 :
Theo bài ra : n+p+e=48(hạt) <=>2p+n=48 (*)
Tổng số hạt mang điện gấp 2 lần số hạt không mang điện <=> 2p=2n=>p=n
Thay vào (*) => 3p=48 => p=n=e =16(hạt)
MA = n+p = 16+16=32(đvC)
Bài 1 :
Nguyên tử sắt có điện tích hạt nhân là 26+ => p = 26 (hạt )(1)
Trong nguyên tử số hạt mang điện nhiều hơn số hạt không mang điện là 22.
=> p + e - n = 22 => 2p - n =22 (2)
Thay (1) vào (2)
52 - n = 22 => n = 30 (hạt )
=> \(A_{Fe}=30+26=56\left(ĐvC\right)\)
Bài 2 :
Nguyên tử M có số nơtron nhiều hơn số proton là 1 ;
\(\left(n-p\right)_M=1=>n=p+1\left(1\right)\)
Số hạt mang điện nhiều hơn số hạt không mang điện là 10.
\(p+e-n=10=>2p-n=10\left(2\right)\)
Thay (1) vào (2) có :
\(2p-p-1=10=>p=11\left(hạt\right)\)
\(=>e=p=11\left(hạt\right);n=12\left(hạt\right)\)
làm r ko cần làm lại đâu . Thà sai r làm lại thì đc
Bài 3 :
Tổng số hạt trong nguyên tử là 28.\(=>p+n+e=28\)
p = e \(=>2p+n=28\left(1\right)\)
Trong đó số hạt không mang điên xấp xỉ 35% .
\(=>n=\dfrac{35}{100}S=\dfrac{35}{100}\left(2p+n\right)=>0,65n=0,7p=>n=\dfrac{14}{13}p\left(2\right)\)
Thay (2) vào (1)
\(=>2p+\dfrac{14}{13}p=28=>p\approx9\left(hạt\right)\)
\(=>e=p=9\left(hạt\right)=>n=10\left(hạt\right)\)