Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1 : Qua nhận xét về phân tử khối và liên kết hidro trong mỗi hợp chất, ta có :
Thứ tự : Axit > Ancol > Este > Hidrocacbon
Ta thấy : Glyxin ở dạng ion lưỡng cực nên có nhiệt độ sôi cao hơn axit propionic
Vậy, theo chiều tăng dần nhiệt độ sôi, nhiệt độ nóng chảy là :
Glyxin > Axit propionic > Butan-1-ol >Metyl axetat > Butan

Fe_______________________Fe2+
Fe3O4______NaHSO4 0,32 \(\rightarrow\)Fe3+_______+NO 0,04 +H2O
Fe(NO3)2 ________________Na+ 0,32
_________________________SO42- 0,32
_________________________NO3-
_________________________53,92g
Theo bảo toàn H: nNaHSO4=2nH2O=0,32
\(\rightarrow\)nH2O=0,16
Theo bảo toàn khối lượng
m+mNaHSO4=m muối+mNO+mH2O
\(\rightarrow\)m+0,32.120=53,92+0,04.30+0,16.18
\(\rightarrow\)m=19,6

104,48gam104,48gam
Giải thích các bước giải:
Sơ đồ phản ứng:
⎧⎪ ⎪ ⎪⎨⎪ ⎪ ⎪⎩AlMgFeOFe3O4+HNO3−−−−−→⎧⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎨⎪ ⎪ ⎪ ⎪ ⎪ ⎪⎩NO,N2OH2O⎧⎪⎨⎪⎩Al(NO3)2Mg(NO3)2Fe(NO3)2to→⎧⎨⎩Al2O3MgOFe2O3+NO2+O2{AlMgFeOFe3O4→+HNO3{NO,N2OH2O{Al(NO3)2Mg(NO3)2Fe(NO3)2→to{Al2O3MgOFe2O3+NO2+O2
Oxi chiếm 20,22%20,22% khối lượng hỗn hợp.
mO=25,32%.25,32=5,12gammO=25,32%.25,32=5,12gam
→nO=0,32mol→nO=0,32mol
Gọi số mol của NONO và N2ON2O lần lượt là xx và yy mol
⎧⎨⎩x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02{x+y=3,58422,4=0,16mol30x+44y=0,16.2.15,875→{x=0,14y=0,02
Quy đổi hỗn hợp X thành các nguyên tố: Al,Mg,Fe,OAl,Mg,Fe,O
→mKl=25,32−5,12=20,2g→mKl=25,32−5,12=20,2g
→mO(cr)=30,92−20,2=10,72gam→mO(cr)=30,92−20,2=10,72gam
→nO=0,67mol→nO=0,67mol
3nAl+3nFe+2nMg=2nO(cr)3nAl+3nFe+2nMg=2nO(cr)
Gọi số mol của NH4NO3NH4NO3 là xx mol
Bảo toàn e:
3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O3nAl+3nFe+2nMg=2nO+8nNH4NO3+3nNO+8nN2O
0,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.80,67.2=2.0,32+8nNH4NO3+3.0,14+0,02.8
→nNH4NO3=0,015mol→nNH4NO3=0,015mol
Khối lượng muối:
m=mKl+mNO−3+mNH4NO3m=mKl+mNO3−+mNH4NO3
=20,2+0,67.2.62+0,015.80=104,48gam
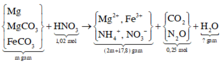
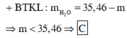
X gồm : CO2(a mol) ; NO(b mol)
Ta có :
a + b= 1
44a + 30b = 1.17,8.2
Suy ra : a = 0,4 ; b = 0,6
Hỗn hợp ban đầu gồm : \(\begin{matrix}FeO:x\left(mol\right)\\Fe\left(OH\right)_2:y\left(mol\right)\\FeCO_3:a=0,4\left(mol\right)\\Fe_3O_4:z\left(mol\right)\end{matrix}\)
Ta có : z = 0,25(x + y + 0,4 + z)
⇒ x + y - 3z + 0,4 = 0(1)
Bảo toàn electron : x + y + 0,4 + z = \(3n_{NO}\)=1,8(2)
Từ (1)(2) suy ra : z = 0,45 ; x + y = 0,95
Phân bổ H+ :
\(2H^++ O^{2-} \to H_2O\\ OH^- + H^+ \to H_2O\\ 2H^+ + O_{trong\ Fe_3O_4}^{2-} \to H_2O\\ CO_3^{2-} + 2H^+ \to CO_2 + H_2O\\ 4H^+ + NO_3^- \to NO + 2H_2O\)
Vậy :
\(n_{HNO_3} = n_{H^+} =(x + y).2 + 8z + 2n_{CO_2} + 4n_{NO}=0,95.2 + 0,45.8 + 0,4.2 + 0,6.4=8,7(mol)\)
cũng đang vướng bài này
Trông nó vậy thôi chứ giải ngắn lắm :3
Toshiro e gặp bài tương tự như này nhưng nó cho hh khí gồm CO2 và NO và tỉ khối khí với H2 là 18,5 , Fe3O4 chiếm 1/3 tổng số mol
:3 Đấy là ý tưởng lớn gặp nhau
Toshiro
Một cách làm vẫn hơi mang hơi hưởng của toán học
Tay quen...
May quá cũng không ế các bác ạ :<
Đáp án:
Ta có: \(n_{NO}=0,6\left(mol\right);n_{CO_2}=0,4\left(mol\right)\)
Nhận thấy tất cả các chất đều cho 1e
Do đó bảo toàn e ta có: \(n_{hh}=3.n_{NO}=3.0,6=1,8\left(mol\right)\)
\(\Rightarrow n_{Fe_3O_4}=0,45\left(mol\right)\Rightarrow\Sigma n_{FeO;Fe\left(OH\right)_2}=0,95\left(mol\right)\)
Nhận thấy \(O;2OH\) đều cần \(2H^+\) để phản ứng
Do đó bảo toàn H+ ta có: \(n_{HNO_3}=4.n_{NO}+2.n_{CO_3^{2-}}+2.\Sigma n_{O;OH}+2.n_O=8,7\left(mol\right)\)
Không bạn đã nhận ra được sự cố tình cho thiếu dữ kiện của bài này là đúng hướng rồi đó :3 Chuẩn bị với #2 nhé
cho t hỏi tí là sao chắc chắn 2 khí không màu đó là CO2 với NO vậy ạ
1 khí là CO2 là chắc chắn rồi nè dựa theo M trung bình và dung dịch HNO3 loãng thì khí còn lại phải là NO