Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Gọi CTHH là \(X_2O_a\)
ta có \(MX_2O_a=6.MH_2O=6.18=108đvc\)
ta lại có
\(\%O=\dfrac{16.a}{108}.100\%=74,1\%=>a\sim5\)
ta có \(2.Mx+5.16=108đvc=>Mx=14đvc\)
vậy X là Nitơ (N)
=> CTHH là \(N_2O_5\)

Đặt CTTQ : FexOy (x,y: nguyên, dương)
mFe=70%.160=112(g) -> x= 112/56=2
mO=160-112=48(g) -> y=48/16=3
=> Với x=2; y=3 => CTHH oxit sắt cần tìm Fe2O3
Chúc em học tốt!

Công thức chung của hợp chất F e x O y .
Theo đề bài ta có:
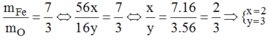
Vậy CTHH của hợp chất là F e 2 O 3 .
Phân tử khối là: 56.2 + 16.3 = 160 (đvC)

Anh thử tham khảo ở câu hỏi này xem sao ạ, khúc sau nó có hơi khác 1 chút ạ
Xác định công thức của các hợp chất sau a) Hợp chất tạo thành bởi magie và oxi có phân tử khối là 40, trong phần trăm về khối lượng của chúng lần lượt là 60%

a. Gọi CTHH của A là: X2Oa
Theo đề, ta có: \(d_{\dfrac{A}{H_2O}}=\dfrac{M_A}{M_{H_2O}}=\dfrac{M_A}{18}=6\left(lần\right)\)
=> MA = 108(g)
Theo đề, ta lại có:
\(\%_{X_{\left(A\right)}}=\dfrac{2M_X}{108}.100\%=100\%-74,1\%=25,9\%\)
=> \(M_X\approx14\left(g\right)\)
=> X là nitơ (N)
Ta lại có: \(PTK_A=14.2+16.a=108\left(đvC\right)\)
=> a = 5
b. CTHH của A là: N2O5
Bài 1 :
Ta có :
\(PTK_A=40\left(\text{đ}vc\right)\Rightarrow M_A=40\left(\dfrac{g}{mol}\right)\)
Đặt CTHH TQ của h/c A là MgxOy
Theo đề ta có :
%mMg=60% => mMg = 24(g) => nMg = 1 (mol)
%mO = 40% => mO = 16 (g) => nO = 1 (mol)
Ta có tỉ lệ :
\(\dfrac{nMg}{nO}=\dfrac{x}{y}=\dfrac{1}{1}\) => \(\left\{{}\begin{matrix}x=1\\y=1\end{matrix}\right.\) Vậy CTHH của h/c A là MgO
Bài 2 :
Theo đề bài ta có : \(PTK_B=160\left(\text{đ}vc\right)hay\) \(M_B=160\left(\dfrac{g}{mol}\right)\)
Đặt CTHHTQ của B là : FexOy
Ta có : %mFe = 70% => mFe = 112 (g) => nFe = 2 (mol)
%mO = 30% => mO = 48 g => nO = 3 (mol)
Ta có tỉ lệ :
\(\dfrac{nFe}{nO}=\dfrac{x}{y}=\dfrac{2}{3}\Rightarrow\left\{{}\begin{matrix}x=2\\y=3\end{matrix}\right.\) Vậy CTHH của h/c B là Fe2O3
Theo đề ta có :
\(PTK_C=2.PTK_{O2}=2.32=64\left(\text{đ}vc\right)hay\) \(M_C=64\left(\dfrac{g}{mol}\right)\)
Đặt CTHH của h/c C là SxOy
Ta có : %mS = 50% => mS = 32(g) => nS = 1 (mol)
%mO = 50% => mO = 32(g) => nO = 2(mol)
Ta có tỉ lệ : \(\dfrac{nS}{nO}=\dfrac{x}{y}=\dfrac{1}{2}\Rightarrow\left\{{}\begin{matrix}x=1\\y=2\end{matrix}\right.\) Vậy CTHH của h/c C là SO2
Theo bài ra :
\(\dfrac{PTK_C}{PTK_{oxi}}=2=>PTK_C=32.2=64\left(ĐvC\right)\)
Trong một mol hợp chất có :
\(m_S=\dfrac{50}{100}.64=32\left(g\right)\)
\(m_O=64-32=32\left(g\right)\)
\(n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(n_O=\dfrac{32}{16}=2\left(mol\right)\)
\(=>CTHH_C:SO_2\)
ủa đá bóng xong r à
Bài 2 :
Theo bài ra ta có :
\(PTK_B=160\left(ĐvC\right)=>M_B=160\left(\dfrac{g}{mol}\right)\)
Trong 1 mol hợp chất có :
\(m_O=\dfrac{30}{100}.160=48\left(g\right)\)
\(m_{Fe}=\dfrac{100-30}{100}.160=112\left(g\right)\)
\(n_O=\dfrac{48}{16}=3\left(mol\right)\)
\(n_{Fe}=\dfrac{112}{56}=2\left(mol\right)\)
\(=>CTHH_B:Fe_2O_3\)
chiều đá h ms đi hc về
đá buổi sáng mà chết à
ể tl nhiều phết
Như Khương Nguyễn tha thu kakakaka
Bài 1 :Theo bài ra ta có :
\(PTK_A=40\left(ĐvC\right)=>M_A=40\left(\dfrac{g}{mol}\right)\)
Trong 1 mol hợp chất có :
\(m_{Mg}=\dfrac{60}{100}.40=24\left(g\right)\)
\(m_O=\dfrac{40}{100}.40=16\left(g\right)\)
\(n_{Mg}=\dfrac{24}{24}=1\left(mol\right)\)
\(n_O=\dfrac{16}{16}=1\left(mol\right)\)
\(=>CTHH_A:MgO\)
ể
sao tui vẫn ko tag tên đc vãi
tl đúng r ko cần tl lại đâu
@Minh Thương dám tl lại mấy câu tui tl r
tui chơi lại
môn lí đó
dám chơi vs tui hả
Như Khương Nguyễn chịu
???
haizzzzzzzzzzzzzzzzzzzzzzzzzz