Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Gọi công thức của hai muối trong hỗn hợp ban đầu là A2CO3 và BCO3.
Có các phản ứng:
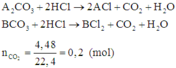
Quan sát phản ứng thấy khi cho hỗn hợp phản ứng với dung dịch HCl thì mỗi gốc C O 3 2 - trong muối được thay thế bởi hai gốc Cl-.
Có 1 mol C O 3 2 - bị thay thế bởi 2 mol Cl- thì khối lượng của muối tăng: (2.35,5 -60) = 11(gam)
Do đó khối lượng muối khan thu được khi cô cạn dung dịch là:
mmuối clorua = mmuối cacbonat + 0,2.11 = 23,8 + 0,2.11= 26 (gam)

Đáp án D
Gọi hóa trị của kim loại là n (1 ; 2 ; 3), Khối lượng mol là a (g)
Gọi số mol muối mỗi phần là x. Ta có số mol kim loại ban đầu là 2x
Có : 2ax = 4,8 nên ax = 2,4 (1)
Nếu muối tạo thành chỉ là M(NO3)n thì ta có : (a + 62n)x = 25,6 (2)
Từ (1) và (2) => x = (25,6 – 2,4)/(62n) = 0,187/n
Mặt khác , số mol oxit thu được là x/2
=> (2a + 16n).x/2 = 4 (3)
Từ (1) và (3) => x = (4 – 2,4)/(16n) = 0,1/n.
2 giá trị x không bằng nhau. Vì vậy muối phải là muối ngậm nước.
Đặt công thức muối là M(NO3)n.mH2O
Khối lượng muối mỗi phần là (a + 62n + 18m)x = 25,6 (4)
Kết hợp (1), (3), (4) ta có hệ sau :
ax = 2,4
(2a + 16n).x/2 = 4
(a + 62n + 18m)x = 25,6
=> nx = 0,2 ; mx = 0,6
=> a/n = 12. Thay n = 1, 2, 3 ta được a = 24g => Mg
Thay n = 2 => x = 0,1 ; do đó m = 6
Vậy M là Mg và muối là Mg(NO3)2.6H2O

1.
X+4HNO3\(\rightarrow\)X(NO3)2+2NO2+2H2O
nNO2=\(\frac{8,96}{22,4}\)=0,4(mol)
\(\rightarrow\)nX=0,2(mol)
MX=\(\frac{12,8}{0,2}\)=64(g/mol)
\(\rightarrow\)X là Cu
2.
8A+30HNO3\(\rightarrow\)8A(NO3)3+3N2O+15H2O
10A+36HNO3\(\rightarrow\)10A(NO3)3+3N2+18H2O
nN2O=a nN2=b
Giải HPT:\(\left\{{}\begin{matrix}\text{44a+28b=36,9.0,27}\\\text{a+b=0,27}\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}\text{a=0,15}\\\text{b=0,12}\end{matrix}\right.\)
\(\rightarrow\)MA=\(\frac{2,16}{0,27}\)=8

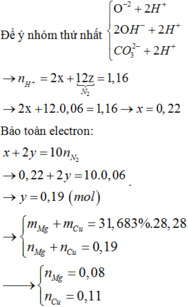

Câu 3:
nNO2 (đktc) = \(\frac{11,44}{22,4}\) = 0,51 (mol)
Đặt số mol của Cu và Zn lần lượt là x và y (mol)
→ mhh = 64x + 65y = 19,4 (I)
Qúa trình nhường e
Cu → Cu+2 + 2e
x___________ 2x (mol)
Mg → Mg+2 + 2e
y ___________2y (mol)
Quá trình nhận e
N+5 + 1e → N+4 (NO2)
_____0,52__0,52 (mol)
Bảo toàn e ta có: ne(KL nhường) = ne(N+5 nhận)
→ 2x + 2y = 0,51 (II)
Giải hệ phương trình (I) và (II) ta có x = ? và y = ?
Tuy nhiên hệ vô nghiệm nên bạn kiểm tra lại đề bài xem có vẫn đề k nhé!
Câu 4:
Dung dịch có khả năng dẫn điện là dd tan trong nước phân li ra cation và anion
Thỏa mãn: NaCl → Na+ + Cl-
B,C,D loại vì chỉ tan trong nước không phân li ra các ion
Đáp án A
1.
gọi kim loại hoá trị I là A
n khí = 10,08/22,4=0,45mol
=> công thức muối nitrat là : ANO3
pt : 2ANO3 ----đp--> 2A + 2NO2 + O2
theo pt ta có : nNO2 = 2nO2
mà nNO2 + nO2 = 0,45
⇔2nO2+nO2=0,45⇔2nO2+nO2=0,45
⇔3nO2=0,45⇔3nO2=0,45
⇔nO2=0,15mol⇔nO2=0,15mol
theo pt ta có : nM = 2nO2 = 2.0,15=0,3mol
=> MA= 32,4/0,3=108
Vậy kim loại hoá trị I là Ag
=> CT : AgNO3
theo pt ta có : nAgNO3 = 2nO2 = 2. 0,15 =0,3mol
mAgNO3 = 0,3.170 = 51g
2.
Vì muối đem nhiệt phân là muối nitrat của kim loại M hóa trị II và phản ứng thu được oxit tương ứng nên sản phẩm thu được là MO.
Áp dụng phương pháp tăng giảm khối lượng: M(NO3)2 → MO
M + 62.2 M + 16
18,8 gam 8 gam
⇒\(\frac{M+124}{18,8}=\frac{M+16}{8}\Rightarrow M=64\)
Vậy kim loại M là Cu.
6. Nguyên nhân tính dẫn điện của dung dịch các chất điện li là
A. Phân tử các chất hòa tan
B. Các ion trong dd
C. Các anion trong dung dịch
D. Các cation trong dung dịch
Vì :Do sự phân ly của các ion cation và ion anion.