Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phản ứng thu nhiệt là: phản ứng (1)
Phản ứng tỏa nhiệt là: phản ứng (2)

1.
Phản ứng ở bình Na2SO3 0,3 M xảy ra nhanh nhất
Phản ứng ở bình Na2SO3 0,05 M xảy ra chậm nhất
2.
Khi nồng độ chất phản ứng tăng lên, số va chạm giữa các hạt tăng lên, làm số va chạm hiệu quả cũng tăng lên và dẫn đến tốc độ phản ứng tăng.

Lần sau đăng chia nhỏ câu hỏi ra nhé
4.
R+H2SO4\(\rightarrow\)RSO4+H2
a) Ta có
nR=nRSO4
\(\rightarrow\)\(\frac{32,88}{R}\)=\(\frac{55,92}{R+96}\)
\(\rightarrow\)\(\text{R=137}\)
\(\rightarrow\)R là Bari(Ba)
b)
nBa=\(\frac{32,88}{137}\)=0,24(mol)
\(\rightarrow\)nH2=nBa=0,24(mol)
\(\text{VH2=0,24.22,4=5,376(l)}\)
nH2SO4=nBa=0,24(mol)
CMH2SO4=\(\frac{0,24}{0,2}\)=1,2(M)
2.
M+H2SO4\(\rightarrow\)MSO4+H2
nH2=\(\frac{4,48}{22,4}\)=0,2(mol)
nM=nH2=0,2(mol)
M=\(\frac{13}{0,2}\)=65(g/mol)
\(\rightarrow\)M là kẽm (Zn)
3.
M+H2SO4\(\rightarrow\)MSO4+H2
nH2=\(\frac{7,84}{22,4}\)=0,35(mol)
M=\(\frac{14}{0,35}\)=40
\(\rightarrow\)M là Canxi
b)
nCaSO4=nH2=0,35(mol)
\(\text{mCaSO4=0,35.136=47,6(g)}\)
 Biến thiên nồng độ trong khoảng thời gian từ 0 giờ đến 3 giờ là:
Biến thiên nồng độ trong khoảng thời gian từ 0 giờ đến 3 giờ là: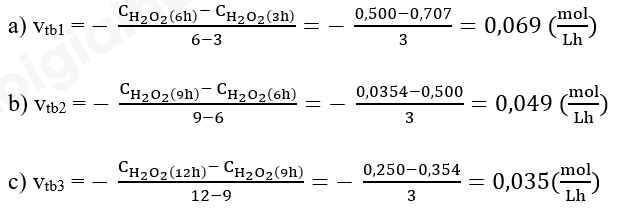



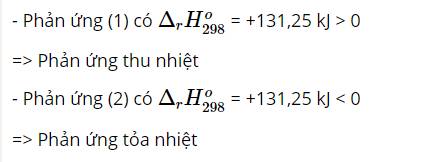
 Quan sát vạch chữ X trên tờ giấy dưới đáy bình, ghi lại thời điểm không nhìn thấy vạch chữ X nữa và trả lời câu hỏi:
Quan sát vạch chữ X trên tờ giấy dưới đáy bình, ghi lại thời điểm không nhìn thấy vạch chữ X nữa và trả lời câu hỏi:
áp dụng công thức
v = ΔC\Δt = 0,22 - 0,1 \ 4 = 0,03 (M\s)�‾=Δ�Δ�=0,22−0,14=0,03(��)
Tốc độ trung bình của phản ứng là: ¯¯¯v=0,22−0,104=0,03(mol/s)
v = ΔC\Δt = 0,22 - 0,1 \ 4 = 0,03 (M\s
File: undefined
v = ΔC\Δt = (0,22 - 0,1 )\ 4 = 0,03 (M\s)
Công thức tính tốc độ phản ứng theo chất tham gia: ¯v=−ΔCΔt
Tốc độ phản ứng sau 4s theo tert-butyl chloride:
¯v=−0,10−0,224=0,03(M/s)
Câu 2
Tốc độ trung bình của phản ứng theo tert — butyl chloride sau 4 giây là
v = 0,22 -0,10/4 = 0,12/4 = 0,03 (m/s)
Tốc độ trung bình của phản ứng theo tert-butyl-chloride là vtb=-0,10-0,22/4=0,12/4=0,03M/s
v=-∆C/∆t=C2-C1/t2-t1
Theo công thức trên,ta có:
v=0,10-0,22/4=-0,12/4=0,03(M/s)
Tốc độ trung bình của phản ứng là 0,03M/s
Công thức tính tốc độ phản ứng theo chất tham gia V=∆C/∆t
Tốc độ phản ứng sau 4s theo tert-butyl chloride:v=-0,10-0,22/4 =0,03 (M/s)
tốc độ trung bình của phản ứng là 0,03 M/s
Tính tốc độ trung bình của phản ứng theo tert-butyl chloride.
Tốc độ trung bình của phản ứng theo một chất được tính bằng sự thay đổi nồng độ của chất đó chia cho khoảng thời gian phản ứng. Đối với chất phản ứng, tốc độ thường được biểu thị bằng giá trị dương, do đó ta lấy giá trị tuyệt đối của sự thay đổi nồng độ.
Tốc độ trung bình $= -\frac{\Delta[C4H9Cl]}{\Delta t}$
Tốc độ trung bình $= -\frac{-0,12 \, M}{4 \, s}$
Tốc độ trung bình $= \frac{0,12 \, M}{4 \, s} = 0,03 \, M/s$
- 𝐶1 =0 , 22 M (nồng độ ban đầu).
- 𝐶2 =0 , 10 M (nồng độ sau 4 giây).
- Δ𝑡 =4 s (khoảng thời gian phản ứng).
Các bước giải chi tiết:- Xác định độ biến thiên nồng độ ( ΔCΔ𝐶):
- Tính tốc độ trung bình ( v̄𝑣̄):
Kết luận:Δ𝐶 =𝐶2 −𝐶1 =0 , 10 −0 , 22 = −0 , 12 M.
v̄=−-0,124=0,03(M/s)𝑣̄=−−0,124=0,03(M/s)
Tốc độ trung bình của phản ứng trong khoảng thời gian 4 giây là 0,03 M/s.
Nồng độ của phản ứng là
0,22 - 0,1 = 0,12
Ta có công thức
Tốc độ TB=nồng độ/thời gian
=0,12/4
=0,03M/s
Vậy tốc độ tb của phản ứng là 0,03M/s