Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

3. CuO +H2SO4 -->CuSO4 +H2O
nCuO=64/80=0,8(mol)
theo PTHH :nCuO =nH2SO4=nCuSO4=0,8(mol)
=>mddH2SO4 20%=0,8.98.100/20=392(g)
mCuSO4=0,8.160=128(g)
mdd sau phản ứng =64 +392=456(g)
mH2O=456 -128=328(g)
giả sử có a g CuSO4.5H2O tách ra
trong 250g CuSO4 tách ra có 160g CuSO4 và 90g H2O tách ra
=> trong a g CuSO4.5H2O tách ra có : 160a/250 g CuSO4 và 90a/250 g H2O tách ra
=>mCuSO4(còn lại)=128 -160a/250 (g)
mH2O (còn lại)=328 -90a/250 (g)
=>\(\dfrac{128-\dfrac{160a}{250}}{328-\dfrac{90a}{250}}.100=25\)
=>a=83,63(g)

a) Nhận xét: 33,84g X > 16g rắn → kim loại còn dư.
Chú ý: sau một thời gian ám chỉ các chất tham gia đều dư.
Giả sử số mol của Mg, Fe lần lượt là x, y
Tăng giảm khối lượng: (64 – 24) . x + (64 – 56) . y = 38,24 – 33,84 (1)
Chất rắn bao gồm MgO: x; Fe2O3: 0,5y; CuO: a – x – y
=> 40x + 160 . 0,5y + 80(a – x – y) = 16 (2)
Từ (1) và (2) => 10a + y = 2,55
amax <=> y = 0 => amax = 0,255
b) giá trị a đạt max thì Fe chưa tham gia pứ.
Giả sử số mol Mg dư là: z (mol) 19,12g Z cho 0,48 mol SO2 → 38,24g Z cho 0,96 mol SO2
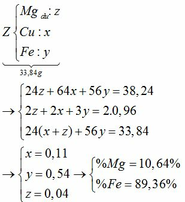

2Al+6HCl---->2AlCl3+3H2
Al2o3+6HCl--->2AlCl3+3H2O
Cu+HCl--> không p/u
2Cu + O2---->2CuO
ncuO=2,75/80=0.034375(mol)
Cứ 2 mol Cu---à 2 mol CuO
0.034375<------0.034375
mCu=0,034375.64=2,2(g)
--->%mCu=2,2.100/10=22%
nH2=3,36/22,4=0,15(mol)
cứ 2 mol Al----->3 mol H2
0.1<-----0.15
mAl :0,1.27=2.7(g)
--->%mAl=2,7.100/10=27%
---->%mAl2o3=100%-27%-22%=51%

a)
$2Cu(NO_3)_2 \xrightarrow{t^o} 2CuO + 4NO_2 + O_2$
Gọi $n_{CuO} = n_{Cu(NO_3)_2\ pư} = a(mol)$
Suy ra:
$m_{giảm} = 188a - 80a = 54 \Rightarrow a = 0,5(mol)$
$m_{Cu(NO_3)_2\ pư} = 0,5.188 = 94(gam)$
b)
$n_{NO_2} = 4a = 2(mol)$
$n_{O_2} = 0,5a = 0,25(mol)$
$V_{NO_2} = 2.22,4 = 44,8(lít)$
$V_{O_2} = 0,25.22,4 = 5,6(lít)$
Bài 1 :
PTHH : 2Cu(NO3)2 -> 2CuO + 4NO2 \(\uparrow\) + O2 \(\uparrow\)
............. \(\dfrac{m}{250}\)................................\(\dfrac{m}{125}\).......\(\dfrac{m}{500}\) (mol)
Gọi khối lượng Cu(NO3)2 đem đi nhiệt phân là m (g)
Theo bài ra ta có hệ :
\(m-m_{NO2\uparrow}-m_{O2\uparrow}=m-0,54\left(g\right)\)
<=> m - \(\left(\dfrac{46m}{125}+\dfrac{32m}{500}\right)=m-0,54\)
<=> \(\dfrac{46m}{125}+\dfrac{32m}{500}=0,54\left(g\right)\)
<=> \(\dfrac{54m}{125}=0,54\left(g\right)\Rightarrow m=1,25\left(g\right)\)
Vậy khối lượng Cu(NO3)2 đem đi nhiệt phân là 1,25 (g)
Bài 1 :
Sửa đề : Nung 17,6g hỗn hợp chất rắn X gồm NaHCO3 và Na2CO3 đến khối lượng không đổi thu được V lít khí hỗn hợp B gồm hơi và khí. Cho hỗn hợp khí hấp thụ hoàn toàn vào Ca(OH)2 dư thì được 12,5g khối lượng kết tủa. Tính thể tích khí và hơi trong V lít hỗn hợp B.
----------------------------------------------------Bài làm---------------------------------------------------------------------
Vì Na2CO3 bền nhiệt nên khi nung nóng sẽ không bị phân hủy
Ta có :
PTHH nung nóng NaHCO3 :
\(2NaHCO3-^{t0}\rightarrow Na2CO3+CO2+H2O\)
Hỗn hợp B thu được bao gồm : H2O (hơi ) và CO2(khí)
Ta có PTHH khi Cho hỗn hợp khí hấp thụ hoàn toàn vào Ca(OH)2 dư :
\(CO2+Ca\left(OH\right)2\rightarrow CaCO3\downarrow+H2O\)
0,125mol..........................0,0125mol
Kết tủa thu được là CaCO3 => mCaCO3=12,5 => nCaCO3=\(\dfrac{12,5}{100}=0,125\left(mol\right)\)
=> \(\left\{{}\begin{matrix}VH2O=0,125.2.22,4=5,6\left(l\right)\\VCO2=0,125.22,4=2,8\left(l\right)\end{matrix}\right.\)
Vậy..............
Tại sao lại phải đổi CaCO3 thành Na2CO3 vậy ?
Nguyễn Xuân Dương tại vì không có hỗn hợp nào bao gồm 2 muối khác loại như bạn
Sửa đề thì cho 17,6g vứt đi đâu? Dữ kiện không bao giờ thừa
Trương Tuyết Nhi mình thấy đề yêu cầu gì thì làm thế