Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. Số nguyên tử Al, số phân tử O2 , số phân tử AL2O3
b. 4Al + 3O2 → 2Al2O3
Tỉ lệ: 4 : 3 : 2

\(Na_2CO_3+Ba\left(OH\right)_2\rightarrow BaCO_3+2NaOH\)
Tỉ lệ: Số phân tử Na2CO3 : Số phân tử Ba(OH)2 : Số phân tử BaCO3 : Số phân tử NaOH = 1:1:1:2
Áp dụng các bước lập phương trình hoá học, cân bằng phương trình.
PTHH: Na2CO3 + Ba(OH)2 → BaCO3 + 2NaOH
Tỉ lệ số phân tử chất trong phản ứng là:
Số phân tử Na2CO3 : số phân tử Ba(OH)2 : số phân tử BaCO3 : số phân tử NaOH = 1 : 1 : 1 : 2

a: \(4Na+O_2\rightarrow2Na_2O\)
=>\(Na:O_2:Na_2O=4:1:2\)
b: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
Tỉ lệ là 1:3:2
c: \(2Fe\left(OH\right)_3\rightarrow Fe_2O_3+3H_2O\)
Tỉ lệ là 2:1:3
d: \(Na_2CO_3+CaCl_2\rightarrow CaCO_3\downarrow+2NaCl\)
Tỉ lệ là 1:1:1:2
Xem lại PT b
P2O5 + 3 H2O -> 2H3PO4 (Tỉ lệ: 1:3:2)

- Sơ đồ của phản ứng hoá học khác với phương trình hoá học ở điểm: sơ đồ hoá học chưa cho biết tỉ lệ về số nguyên tử hoặc số phân tử giữa các chất trong phản ứng. Sơ đồ phản ứng dùng mũi tên đứt, còn PTHH dùng mũi tên liền.
- Ý nghĩa của phương trình hoá học: Phương trình hoá học cho biết trong phản ứng hoá học, lượng các chất tham gia phản ứng và các chất sản phẩm tuân theo một tỉ lệ xác định.

- muối tác dụng với kim loại tạo ra muối mới và kim loại mới (với kim loại tham gia phản ứng mạnh hơn kim loại có trong muối)
- muối tác dụng với aicd tạo thành muối mới và acid mới (với sản phẩm là chất khí, chất kết tủa hoặc nước)
- muối tác dụng với base tạo thành muối mới và base mới (với sản phảm là chất khí, chất kết tủa hoặc nước)
- muối tác dụng với muối tạo thành 2 muối mới (với sản phẩm là chất khí, chất kết tủa hoặc nước)

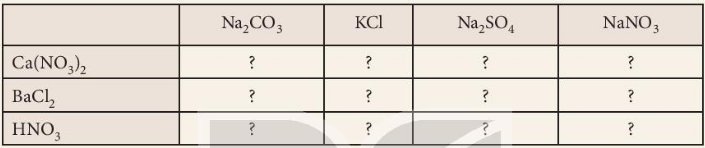
| Na2CO3 | KCl | Na2SO4 | NaNO3 | |
| Ca(NO3)2 | Có phản ứng (1) | Không phản ứng | Có phản ứng (2) | Không phản ứng |
| BaCl2 | Có phản ứng (3) | Không phản ứng | Có phản ứng (4) | Không phản ứng |
| HNO3 | Có phản ứng (5) | Không phản ứng | Không phản ứng | Không phản ứng |
Các PTHH:
\(\left(1\right)Ca\left(NO_3\right)_2+Na_2CO_3\rightarrow2NaNO_3+CaCO_3\downarrow\\ \left(2\right)Na_2SO_4+Ca\left(NO_3\right)_2\rightarrow CaSO_4+2NaNO_3\\ \left(3\right)Na_2CO_3+BaCl_2\rightarrow BaCO_3+2NaCl\\ \left(4\right)Na_2SO_4+BaCl_2\rightarrow BaSO_4+2NaCl\\ \left(5\right)2HNO_3+Na_2CO_3\rightarrow2NaNO_3+CO_2+H_2O\)

\(SO_2+2NaOH\rightarrow Na_2SO_4+H_2O\\ SO_2+NaOH\rightarrow NaHSO_3\)

Phương trình hoá học: 4Al + 3O2 → 2Al2O3.
Số mol Al tham gia phản ứng:
n Al = mAl : M Al = 0,54 : 27 = 0,02 mol
a) Từ phương trình hóa học ta có:
n Al2O3 = ½ n Al = 0,02 : 2 = 0,01 mol
n Al2O3 = 0,01 x 102 = 10,2 gam
b) theo phương trình hóa học ta có:
n O2 = ¾ n Al = ¾ x 0,02 = 0,015 mol
V O2 (đkc) = 0,015 x 24,79 = 0,37185 (lít)
\(PTHH:4Al+3O_2\left(t^o\right)\rightarrow2Al_2O_3\\ n_{Al}=\dfrac{0,54}{27}=0,02\left(mol\right)\Rightarrow n_{Al}=\dfrac{2}{4}.0,02=0,01\left(mol\right);n_{O_2}=\dfrac{3}{4}.0,02=0,15\left(mol\right)\\ a,m_{Al_2O_3}=0,01.27=0,27\left(g\right)\\ b,V_{O_2\left(đkc\right)}=0,15.24,79=3,7185\left(l\right)\)

PTHH :
\(a,Fe+CuSO_4\rightarrow FeSO_4+Cu\)
\(b,Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\)

1. Định nghĩa về Oxide:
- Oxide là hợp chất hóa học được hình thành khi một nguyên tố kết hợp với oxy. Trong đó, oxy luôn giữ hóa trị -2 (ngoại trừ trong một số oxide đặc biệt như peroxide hay ozon).
- Công thức chung của một oxide là:
\(X_{n} O_{m}\)
Trong đó \(X\) là nguyên tố, \(n\) và \(m\) là số nguyên dương chỉ số lượng nguyên tử của \(X\) và oxy trong phân tử oxide.
2. Phân loại Oxide theo thành phần nguyên tố:
a. Oxide kim loại (Oxide của kim loại):
- Oxide này được tạo thành từ một kim loại kết hợp với oxy.
- Ví dụ:
- FeO (oxit sắt(II)): Sắt là kim loại kết hợp với oxy.
- Na₂O (oxit natri): Natri là kim loại kiềm kết hợp với oxy.
- CaO (oxit canxi): Canxi là kim loại kiềm thổ kết hợp với oxy.
b. Oxide phi kim (Oxide của phi kim):
- Oxide phi kim được tạo thành khi một phi kim kết hợp với oxy.
- Ví dụ:
- CO₂ (carbon dioxide): Cacbon là phi kim kết hợp với oxy.
- SO₂ (sulfur dioxide): Lưu huỳnh là phi kim kết hợp với oxy.
- NO₂ (nitrogen dioxide): Nitơ là phi kim kết hợp với oxy.
3. Phân loại Oxide theo tính chất hóa học:
Dựa trên tính chất hóa học, oxide có thể được chia thành bốn loại chính: oxide acid, oxide base, oxide lưỡng tính, và oxide trung tính.
a. Oxide acid:
- Tính chất: Oxide acid khi tác dụng với nước sẽ tạo thành axit. Chúng chủ yếu là oxide của phi kim.
- Ví dụ:
\(C O_{2} + H_{2} O \rightarrow H_{2} C O_{3}\)
\(S O_{2} + H_{2} O \rightarrow H_{2} S O_{3}\) - CO₂ (carbon dioxide): Khi CO₂ tác dụng với nước, tạo thành axit cacbonic (H₂CO₃).
- SO₂ (sulfur dioxide): Khi SO₂ tác dụng với nước, tạo thành axit sulfurous (H₂SO₃).
- Đặc điểm: Oxide acid có tính axit, thường tan trong nước tạo thành dung dịch axit.
b. Oxide base:
- Tính chất: Oxide base khi tác dụng với nước sẽ tạo thành dung dịch kiềm (base). Chúng chủ yếu là oxide của kim loại kiềm hoặc kim loại kiềm thổ.
- Ví dụ:
\(N a_{2} O + H_{2} O \rightarrow 2 N a O H\)
\(C a O + H_{2} O \rightarrow C a \left(\right. O H \left.\right)_{2}\) - Na₂O (oxit natri): Khi Na₂O tác dụng với nước, tạo thành natri hydroxide (NaOH), một base.
- CaO (oxit canxi): Khi CaO tác dụng với nước, tạo thành canxi hydroxide (Ca(OH)₂), một base.
- Đặc điểm: Oxide base có tính kiềm, thường tác dụng với axit tạo thành muối và nước.
c. Oxide lưỡng tính:
- Tính chất: Oxide lưỡng tính có thể vừa tác dụng với axit để tạo thành muối, vừa tác dụng với base tạo thành muối. Chúng có tính chất vừa giống oxide acid, vừa giống oxide base.
- Ví dụ:
\(A l_{2} O_{3} + 6 H C l \rightarrow 2 A l C l_{3} + 3 H_{2} O\)\(A l_{2} O_{3} + 2 N a O H + 3 H_{2} O \rightarrow 2 N a \left[\right. A l \left(\right. O H \left.\right)_{4} \left]\right.\) - Al₂O₃ (oxit nhôm): Khi tác dụng với axit (HCl), Al₂O₃ tạo thành muối nhôm clorua (AlCl₃); khi tác dụng với base (NaOH), Al₂O₃ tạo thành muối aluminate.
- Đặc điểm: Oxide lưỡng tính có tính chất hóa học phức tạp, có thể tham gia vào cả phản ứng axit và base.
d. Oxide trung tính:
- Tính chất: Oxide trung tính không có tính axit cũng không có tính kiềm, và không tác dụng với nước hoặc với axit/base.
- Ví dụ:
- CO (carbon monoxide): CO không tác dụng với nước và cũng không tạo ra phản ứng với axit hoặc base.
- N₂O (nitrous oxide): N₂O cũng không có tính axit hay base rõ rệt.
- Đặc điểm: Oxide trung tính không làm thay đổi độ pH của dung dịch và không tham gia vào phản ứng axit-base.
Tóm tắt:
- Định nghĩa: Oxide là hợp chất của hai nguyên tố, trong đó có một nguyên tố là oxy.
- Phân loại theo thành phần nguyên tố:
- Oxide kim loại: Oxide của các kim loại (Na₂O, FeO, CaO).
- Oxide phi kim: Oxide của các phi kim (CO₂, SO₂, NO₂).
- Phân loại theo tính chất hóa học:
- Oxide acid: Tác dụng với nước tạo thành axit (CO₂, SO₂).
- Oxide base: Tác dụng với nước tạo thành kiềm (Na₂O, CaO).
- Oxide lưỡng tính: Có thể tác dụng với cả axit và base (Al₂O₃).
- Oxide trung tính: Không có tính axit hay kiềm, không tác dụng với axit hay base (CO, N₂O).
Câu 1. Phương trình hoá học là cách biểu diễn ngắn gọn phản ứng hoá học bằng công thức hoá học của các chất tham gia và sản phẩm, kèm theo hệ số thích hợp.
Câu 2. Khi lập phương trình hoá học, số nguyên tử của mỗi nguyên tố ở hai vế phải bằng nhau.
Câu 3. Phương trình hoá học cho biết:
Câu 4. Vì trong phản ứng hoá học, nguyên tử không tự sinh ra hay mất đi, nên phải cân bằng số nguyên tử ở hai vế.
Câu 5. Dựa vào phương trình hoá học, ta xác định được tỉ lệ giữa các chất theo số mol