Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1)
a) 2HgO\(-t^0\rightarrow2Hg+O_2\)
b)Theo gt: \(n_{HgO}=\frac{2,17}{96}\approx0,023\left(mol\right)\\ \)
theo PTHH : \(n_{O2}=\frac{1}{2}n_{HgO}=\frac{1}{2}\cdot0,023=0,0115\left(mol\right)\\ \Rightarrow m_{O2}=0,0115\cdot32=0,368\left(g\right)\)
c)theo gt:\(n_{HgO}=0,5\left(mol\right)\)
theo PTHH : \(n_{Hg}=n_{HgO}=0,5\left(mol\right)\\ \Rightarrow m_{Hg}=0,5\cdot80=40\left(g\right)\)
Câu 2)
a)PTHH : \(S+O_2-t^0\rightarrow SO_2\)
b)theo gt: \(n_{SO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
theo PTHH \(n_S=n_{SO2}=0,1\left(mol\right)\\ \Rightarrow m_S=0,1\cdot32=3,2\left(g\right)\)
Ta có khối lượng S tham gia là 3,25 g , khối lượng S phản ứng là 3,2 g
Độ tinh khiết của mẫu lưu huỳnh là \(\frac{3,2}{3,25}\cdot100\%\approx98,4\%\)
c)the PTHH \(n_{O2}=n_{SO2}=0,1\left(mol\right)\Rightarrow m_{O2}=0,1\cdot32=3,2\left(g\right)\)

Phương trình hóa học CaCO3 → CaO + CO2.
a) nCaO = 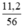 = 0,2 mol.
= 0,2 mol.
Theo PTHH thì nCaCO3 = nCaO = 0,2 (mol)
b) nCaO = 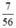 = 0,125 (mol)
= 0,125 (mol)
Theo PTHH thì nCaCO3 = nCaO = 0,125 (mol)
mCaCO3 = M.n = 100.0,125 = 12,5 (g)
c) Theo PTHH thì nCO2 = nCaCO3 = 3,5 (mol)
VCO2 = 22,4.n = 22,4.3,5 = 78,4 (lít)
d) nCO2 = 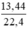 = 0,6 (mol)
= 0,6 (mol)
Theo PTHH nCaO = nCaCO3 = nCO2 = 0,6 (mol)
mCaCO3 = n.M = 0,6.100 = 60 (g)
mCaO = n.M = 0,6.56 = 33,6 (g)

nFe = 0,125 mol
Fe + 2HCl =. FeCl2 + H2
a. nFeCl2 = nFe = 0,125 mol => mFeCl2 = 127.0,125 = 15,875 (g)
b. nH2 = nFe= 0,125 => VH2 = 0,125.22,4 = 2,8(l)
c. áp dụng ĐLBTKL
m chất tham gia = mFeCl2 + mH2 = 15,875 + 0,125.2 = 16,125(g)
Số mol của Fe là :
n=m/M=7/56=0125(mol)
Fe + 2HCl ----> FeCl2 + H2
1mol 2mol 1mol 1mol
0,125mol ----->0,125mol->0,125mol
a) Klg của FeCl2 là :
m=n*M=0,125*127=15,875(g)
b) VH2=n*22,4=0,125*22,4=2,8(l)
c) áp dụng định luật bảo toàn khối lượng ta có :
m chất tham gia =mFeCl2 + mH2=15,875+0,25=16,125(g)

Bài 1:
3NaOH + FeCl3 → 3NaCl + Fe(OH)3↓
\(n_{NaOH}=\frac{20}{40}=0,5\left(mol\right)\)
a) Theo PT: \(n_{FeCl_3}=\frac{1}{3}n_{NaOH}=\frac{1}{3}\times0,5=\frac{1}{6}\left(mol\right)\)
\(\Rightarrow m_{FeCl_3}=\frac{1}{6}\times162,5=27,083\left(g\right)\)
b) Theo pT: \(n_{NaCl}=n_{NaOH}=0,5\left(mol\right)\)
\(\Rightarrow m_{NaCl}=0,5\times58,5=29,25\left(g\right)\)
Theo pT: \(n_{Fe\left(OH\right)_3}=n_{FeCl_3}=\frac{1}{6}\left(mol\right)\)
\(\Rightarrow m_{Fe\left(OH\right)_3}=\frac{1}{6}\times107=17,83\left(g\right)\)
Bài 2:
CaCO3 \(\underrightarrow{to}\) CaO + H2O
a) \(n_{CaO}=\frac{11,2}{56}=0,2\left(mol\right)\)
Theo PT: \(n_{CaCO_3}=n_{CaO}=0,2\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,2\times100=20\left(g\right)\)
b) \(n_{CaO}=\frac{35}{56}=0,625\left(mol\right)\)
Theo PT: \(n_{CaCO_3}=n_{CaO}=0,625\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=0,625\times100=62,5\left(g\right)\)
c) Theo pT: \(n_{CO_2}=n_{CaCO_3}=0,5\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,5\times22,4=11,2\left(l\right)\)
d) \(n_{CO_2}=\frac{33,6}{22,4}=1,5\left(mol\right)\)
Theo pT: \(n_{CaCO_3}=n_{CO_2}=1,5\left(mol\right)\)
\(\Rightarrow m_{CaCO_3}=1,5\times100=150\left(g\right)\)
Theo pT: \(n_{CaO}=n_{CO_2}=1,5\left(mol\right)\)
\(\Rightarrow m_{CaO}=1,5\times56=84\left(g\right)\)

TL
1/ nAl = 5,4 : 27 = 0,2(mol)
4Al + 3O2 ---> 2Al2O3
0,2 ----> 0,1 (mol)
=> mAl2O3 = 0,1 x ( 27 x 2 + 16 x 3 ) = 0,2 x 102 = 20.4 (g)
2/ nAl2O3 = 30,6 : 102 = 0,3 (mol)
4Al + 3O2 ---> 2Al2O3
0,6 <---- 0,3 (mol)
=> mAl = 0,6 x 27 = 16,2 (g)
3/ B1 : Viết phương trình
B2 : Tính số mol các chất
B3 : Dựa vào phương trình hóa học tính được số mol chất cần tìm
B4 : Tính khối lượng.
Áp dụng: 1. C
2. B
3. B
Khi nào rảnh vào kênh H-EDITOR xem vid nha!!! Thanks!

a, \(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
b, Gọi: mO2 = x (g) ⇒ mAl = 1,5x (g)
Theo ĐLBT KL, có: mAl + mO2 = mAl2O3
⇒ 1,5x + x = 10
⇒ x = 4 (g) = mO2
mAl = 1,5.4 = 6 (g)

viết pt, nzn, nhcl; lập tỉ lệ; xác định chất dư (chất có số mol lớn);mzncl2; mh2 theo chất hết.

Ta có: \(n_{Cu}=\dfrac{0,32}{64}=0,005\left(mol\right)\)
a, PTHH: CuO + H2 -to-> H2 + CuO
b, Ta có: \(n_{CuO}=n_{H_2}=n_{Cu}=0,005\left(mol\right)\)
=> \(m_{CuO}=0,005.80=0,4\left(g\right)\)
c) \(V_{H_2\left(đktc\right)}=0,005.22,4=0,112\left(l\right)\)

h2o
Phương trình:
\(2 K C l O_{3} \rightarrow 2 K C l + 3 O_{2}\)a)
\(2\) mol \(K C l O_{3} \rightarrow 3\) mol \(O_{2}\)
\(1,5\) mol \(K C l O_{3} \rightarrow 2,25\) mol \(O_{2}\)
b)
\(0,1\) mol \(K C l O_{3} \rightarrow 0,15\) mol \(O_{2}\)
\(m_{O_{2}} = 0,15 \times 32 = 4,8\) g
Kết quả:
a) \(2,25\) mol \(O_{2}\)
b) \(4,8\) g \(O_{2}\)