Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Dễ thấy cả 2 axit đều có 2 H => HCOOH và HCOO - COOH
Đặt số mol 2 chất là x và y,đặt a = 1 thì
x + y = 1
x + 2y = 1,4
=> x = 0,6 ; y = 0,4
=> %mHCOOH = 43,4%

Bạn coi lại đề chứ mình giải kỹ lắm rồi nhưng nó là kết quả khác.
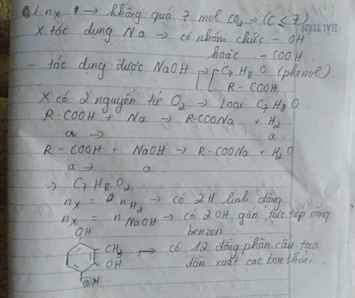

Gọi x = nAg → nCu = 4x → 64.4x + 108x = 1,82 → x = 0,005
nH2SO4 = 0,015 mol; nHNO3 = 0,06 mol → nH+ = 0,09 mol; nNO3- = 0,06 mol
3Cu + 8H+ + 2NO3-
→
3Cu2+ + 2NO + 4H2O
0,02 →
0
,
04
3
3Ag + 4H+ + NO3-
→
3Ag+ + NO + 2H2O
0,005 →
0
,
005
3
→ a = 0 , 04 3 + 0 , 005 3 = 0,015 mol
4NO + 3O2 + 2H2O → 4HNO3
(0,015) (0,1) → 0,015 mol
→ [H+] = [HNO3] = 0,015/0,15 = 0,1M → z = pH = -lg(0,1) = 1
Đáp án D

Đáp án C
Ở bài toán này ta phải sử dụng tổng hợp các tính chất của anđehit.
Khi cho hỗn hợp X tác dụng với Br2 trong CC14 ta thấy Br2 chỉ tác dụng vào liên kết đôi mà không tác dụng vào chức -CHO
msản phẩm hữu cơ m X + m B r 2
Lại có: m B r 2 = n B t r o n g X . Do đó việc ta cần làm là xác định công thức và số mol của 2 anđehit.
Ta có: n A g = 0 , 3 ( m o l ) ; n C O 2 = 0 , 35 ( m o l ) = n C O 2 k h i đ ố t c h á y a n d e h i t
Như các bài toán về phản ứng tráng bạc của anđehit ta phải xét xem hỗn hợp ban đầu có HCHO không. Ta xét 2 trường hợp:
- TH1: A là HCHO. Gọi số mol A và B trong mối phần là nA = a(mol); nB = b(mol)
a = 2 b 4 a + 2 b = 0 , 3 ⇒ a = 0 , 06 ( m o l ) b = 0 , 03 ( m o l )
⇒ n C O 2 d o đ ố t c h á y A = 0 , 06 ( m o l ) ⇒ n C O 2 d o đ ố t c h á y B = 0 , 29 ( m o l ) ⇒ C B = 0 , 29 0 , 03 = 29 3 ( k h ô n g t h ỏ a m ã n )
- TH2: A không phải HCHO. Gọi số mol A và B trong mối phần là nA = a(mol); nB = b(mol)
a = 2 b 2 a + 2 b = 0 , 3 ⇒ a = 0 , 1 ( m o l ) b = 0 , 05 ( m o l ) ⇒ C ¯ = 0 , 35 0 , 15 = 2 , 33
Vì B có ít nhất 3 nguyên tử C trong phân tử
A có 2 nguyên tử C A là CH3CHO
⇒ n C O 2 d o đ ố t c h á y A = 0 , 2 m o l ⇒ n C O 2 d o đ ố t c h á y B = 0 , 15 ( m o l )
⇒ C B = 3 =>B là C2H3CHO
Vậy m s ả n p h ẩ m h ữ u c ơ m A + m B + m C = 0 , 2 . 44 + 0 , 1 . 56 + 1 , 1 . 160 = 30 , 4 ( g )

Đáp án B
Phương pháp:
Bảo toàn electron
Bảo toàn điện tích
Bảo toàn nguyên tố Fe, O, H
Hướng dẫn giải:
Phần kết tủa có nAgCl= 0,3 => nAg = 0,009
Bảo toàn electron: nFe2+ = nAg + 3nNO = 0,036
nNO = 0,009 => nH+ dư = 4nNO = 0,036
Đặt a, b, c là số mol Fe, Fe3O4, Fe(NO3)2 trong X
=> mX = 56a + 232b + 180c = 7,488 (1 )
Dung dịch Y còn H+ dư và Fe2+ nên NO3- đã hết.
Vậy Y chứa Fe2+ (0,036), H+ (0,036), Cl- (0,3)
Bảo toàn điện tích => nFe3+ = 0,064
Bảo toàn Fe => a + 3b + c = 0,064 + 0,036 (2)
Bảo toàn H => nH2O = 0,144
Bảo toàn O:
4nFe3O4 + 6nFe(NO3)2 + 3nHNO3 = nZ + nH2O
=> 4b + 6c + 0,024 . 3 = 0,032 + 0,144 (3)
Giải hệ (1)(2)(3): a = 0,05 b = 0,014 c = 0,008
=> %Fe = 37,4%

Đáp án D
n H 2 O > n C O 2
ancol ban đầu no, đcm chức, mạch hở; n a n c o l d ư = n H 2 O - n C O 2 = 0 , 15 ( m o l )
Lại có: nanđehit = n H 2 O t ạ o t h à n h k h i a n c o l p h ả n ứ n g v ớ i C u O = 0,25 (mol)
⇒ n Y = 0 , 4 ( m o l ) ⇒ C Y ¯ = 1 , 25
Vì X gồm 2 ancol kế tỉếp nhau
=> X1 là CH3OH; X2 là C2H5OH
=> 2 anđehit tương ứng là HCHO và CH3CHO.
Bảo toàn nguyên tố C ta lại có:
n C O 2 = a + 2 b + c + 2 d ⇒ c + 2 d = 0 , 2 ( m o l ) ( 2 )
Từ (1) và (2)
c = 0 , 1 ( m o l ) ; d = 0 , 05 ( m o l ) ⇒ n C H 3 O H b a n đ ầ u = 0 , 3 ( m o l ) ; n C 2 H 5 O H b a n đ ầ u = 0 , 1 ( m o l )
Vậy hiệu suất tạo anđehit của X1
C H 3 O H = 0 , 2 0 , 3 = 66 , 67 %
Hiệu suất tạo anđehit của X2
C 2 H 5 O H = 0 , 05 0 , 1 = 50 %


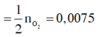
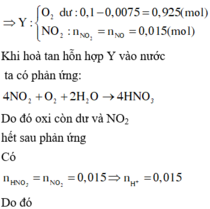
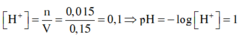

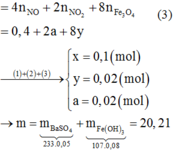
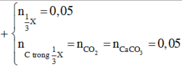
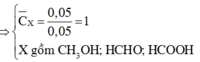
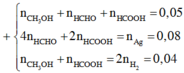
GIẢI CHI TIẾT
Gọi hỗn hợp X gồm:
Tổng số mol:
\(N + U + A = 1\)(1) Phản ứng với Br₂ trong CCl₄
0,5 mol X dùng 2 mol Br₂ (vì 1 mol dư → 3 – 1 = 2 mol phản ứng)
→ Số mol liên kết π có khả năng cộng Br₂ trong 0,5 mol X = 2,
Trong 1 mol X = 4 liên kết π phản ứng được.
Aromatic không cộng Br₂ → không tính ở đây.
(2) Đốt cháy 0,5 mol X → 1.6 mol CO₂, 1.8 mol H₂O
Suy ra tổng nguyên tử:
→ Trung bình gần giống C₃H₇ (xấp xỉ ankan → không cho thông tin lệch nhiều)
(3) Phản ứng với KMnO₄/H⁺
0,5 mol X làm KMnO₄ bị khử tương ứng 0.3 mol O.
Trong cơ chế của chương trình phổ thông:
→ Số mol liên kết π bị oxi hóa trong 0,5 mol X = 0.3
→ Trong 1 mol X = 0.6 liên kết π
(4) Hydrogen hoá: 0,5 mol X → 0,6 mol Y
Số mol tăng:
\(0.6 - 0.5 = 0.1 \&\text{nbsp};\text{mol}\)Khi hydro hoá liên kết π, số mol phân tử không đổi.
Việc số mol tăng chứng tỏ có hydro hoá vòng thơm → từ 1 phân tử thành cyclohexan, số mol KHÔNG tăng.
Như vậy sự tăng 0.1 mol Y không thể xảy ra chỉ do cộng H₂ → Đây là dấu hiệu X có ankyn (cộng 2 H₂ → sản phẩm khác anken → ankan) ⇒ mỗi lần cộng 2H₂ vẫn không làm tăng số phân tử.
Tăng số mol chỉ xảy ra khi hợp chất vòng bị phá vỡ, nhưng với Ni, t° thì vòng thơm không bị mở.
➡️ Điều kiện tăng số mol là do:
hydro hoá đa liên kết trong cùng phân tử → phân tử bền hơn → không làm thay đổi số mol.
Như vậy dựa vào dữ kiện tăng 0.1 mol không rút ra được số mol H₂.
Ta chỉ biết:
\(n_{H_{2}} = \text{s} \overset{ˊ}{\hat{\text{o}}} \&\text{nbsp};\text{li} \hat{\text{e}} \text{n}\&\text{nbsp};\text{k} \overset{ˊ}{\hat{\text{e}}} \text{t}\&\text{nbsp};\pi\&\text{nbsp};\text{c} \overset{ˊ}{\text{o}} \&\text{nbsp};\text{kh}ả\&\text{nbsp};\text{n} \overset{ }{\text{a}} \text{ng}\&\text{nbsp};\text{hydro}\&\text{nbsp};\text{ho} \overset{ˊ}{\text{a}} = 4 \&\text{nbsp};(\text{t}ừ\&\text{nbsp};\text{ph}ả\text{n}\&\text{nbsp};ứ\text{ng}\&\text{nbsp};\text{Br}_{2})\)Nhưng phản ứng xảy ra với 0.5 mol X, nên:
\(n_{H_{2}} = 2 \&\text{nbsp};\text{mol}\)chứ không phải 0.2 mol.
(5) Phản ứng với Na/Etanol giải phóng 0.1 mol H₂
Na chỉ phản ứng với H–C≡C–H hoặc –OH của phenol/alcol.
Ở đây là hiđrocacbon → chỉ có ankyn đầu mạch (H–C≡C–).
1 mol ankyn đầu → 0.5 mol H₂.
0.1 mol H₂ → số mol ankyn đầu = 0.2 mol trong 0.5 mol X
→ Trong toàn bộ 1 mol X = 0.4 mol ankyn đầu.
ĐÁNH GIÁ CÁC NHẬN ĐỊNH
1. X chứa hiđrocacbon thơm đơn nhân
Sai.
Không có dữ kiện nào bắt buộc có vòng benzen. "Thơm" có thể là thơm đa vòng hoặc không nhất thiết phải bị hydrogen hoá. Không buộc.
→ Sai
2. Trong X, số mol hiđrocacbon no = số mol hiđrocacbon không no
Sai.
Không có quan hệ nào từ dữ kiện bắt buộc N = U.
→ Sai
3. Tất cả hiđrocacbon không no trong X đều cộng được Br₂
Đúng.
Br₂ phản ứng hết (chỉ dư 1 mol trong 3 mol ban đầu) và số mol Br₂ phản ứng tương ứng đúng bằng số liên kết π "không thơm".
→ Đúng
4. Sau hidro hoá, số mol H₂ đã dùng bằng 0.2 mol
Sai.
Chúng ta tìm được trong 0.5 mol X có 2 liên kết π (từ 2 mol Br₂), nghĩa là dùng 2 mol H₂, không phải 0.2 mol.
→ Sai
5. Lượng H₂ thoát ra với Na/etanol dùng để xác định số liên kết π trong X
Sai.
Na chỉ phản ứng với ankyn đầu mạch, không phản ứng với nối đôi hay ankyn không đầu.
Vì vậy không thể dùng lượng H₂ với Na để xác định tổng số π.
→ Sai
➡️ Chỉ có 1 nhận định đúng: số 3
Đáp án: A. 1
Chào bạn, đây là một bài toán tổng hợp khá hay về hidrocacbon. Ta sẽ phân tích từng thí nghiệm để xác định thành phần của hỗn hợp X (cho 0,5 mol).
🧪 Phân tích Thí nghiệm (cho 0,5 mol X)
Gọi số mol các thành phần trong 0,5 mol hỗn hợp X là:
1. Phản ứng với $\text{Br}_2$ (Xác định liên kết $\pi_{\text{C=C}}$)
Phản ứng cộng $\text{Br}_2$ chỉ xảy ra với liên kết $\pi$ mạch hở (liên kết $\pi_{\text{C=C}}$) của hiđrocacbon không no. Các hiđrocacbon thơm không phản ứng cộng $\text{Br}_2$ trong điều kiện $\text{CCl}_4$.
$$n_{\text{liên kết } \pi_{\text{C=C}}} = n_{\text{Br}_2} = 2 \text{ mol}$$2. Đốt cháy (Xác định số C, H)
Theo công thức đốt cháy, $n_{\text{ankane}} = n_{\text{H}_2\text{O}} - n_{\text{CO}_2}$. $$\implies n_{\text{no}} = 0,2 \text{ mol}$$
3. Phản ứng với $\text{KMnO}_4/\text{H}^+$ (Xác định liên kết $\pi$ và nhóm thế)
Lượng $\text{KMnO}_4$ bị khử tương ứng với 0,3 mol O. Theo định luật bảo toàn electron, lượng $\text{KMnO}_4$ bị khử tương đương với lượng chất không no phản ứng.
Phản ứng này xảy ra với liên kết đôi/ba (trong $\text{HC}_{\text{kno}}$) và nhánh bên của vòng thơm (trong $\text{HC}_{\text{thơm}}$).
Phản ứng $n_{\text{KMnO}_4} \approx 0,12$ mol không trực tiếp giúp giải quyết câu hỏi, ta sẽ quay lại nếu cần.
4. Hiđro hóa ($\text{H}_2$/$\text{Ni}$, $\text{t}^\circ$)
- Sản phẩm $\text{Y}$ (chỉ $\text{HC}_{\text{no}}$): $n_Y = 0,6$ mol.
- Tổng số mol HC trong $\text{X}$ là $0,5$ mol.
- Phản ứng hiđro hóa chuyển $\text{HC}_{\text{kno}}$ và $\text{HC}_{\text{thơm}}$ thành $\text{HC}_{\text{no}}$.
$$n_Y = n_X + n_{\text{H}_2 \text{ phản ứng}}$$ $$0,6 = 0,5 + n_{\text{H}_2 \text{ pứ}} \implies n_{\text{H}_2 \text{ pứ}} = 0,1 \text{ mol}$$5. Phản ứng với $\text{Na}/\text{etanol}$
💡 Tổng hợp và Kiểm tra Nhận định (cho 0,5 mol X)
Ta có các kết quả chính:
‼️ Phải xem lại Thí nghiệm 1:
Sự mâu thuẫn này chỉ ra rằng đề bài đã cho thí nghiệm 1 sai với dữ kiện $n_{\text{H}_2 \text{ pứ}}$ (TN 4) hoặc đây là lỗi đánh máy trong dữ kiện TN 1.
$\implies n_{\text{Br}_2 \text{ còn lại}} = 3 - 0,1 = 2,9$ mol. (Không phù hợp với $1$ mol $\text{Br}_2$ còn lại).
$\implies n_Y = 0,5 + 2 = 2,5$ mol. (Không phù hợp với $0,6$ mol $\text{Y}$).
Giả định sửa đề (theo logic bài toán ĐH): Dữ kiện TN 1 là lỗi đánh máy hoặc dữ kiện gây nhiễu/dư thừa không dùng được. Ta sẽ dựa vào các dữ kiện có tính logic và chặt chẽ hơn (TN 2, 4, 5) để giải quyết bài toán.
Sử dụng TN 2, 4, 5:
Kết luận thành phần $0,5$ mol X:
📝 Đánh giá các Nhận định
1. Hỗn hợp X chắc chắn chứa một hiđrocacbon thơm đơn nhân.
toàn dùng chat skibidi thế này