Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
viết một bài luận văn nói về ô nhiễm không khí có liên quan đến sự biến đổi của một số chất hóa học.


Đáp án D
Hợp chất Y được cấu tạo từ ion M+ và ion X- Hợp chất Y là MX
Theo giả thiết ta có:
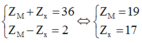
=> M là Kali và X là Cl
K có cấu hình electron là: 1s22s22p63s23p64s1
=> K thuộc chu kì 4; nhóm IA
Cl có cấu hình electron là: 1s22s22p63s23p5
=> Cl thuộc chu kì 3; nhóm VIIA

Đáp án D
Hợp chất Y được cấu tạo từ ion M+ và ion X-
⇒ Hợp chất Y là MX
Theo giả thiết ta có:

⇒ M là Kali và X là Cl
K có cấu hình electron là: 1s22s22p63s23p64s1
⇒ K thuộc chu kì 4; nhóm IA
Cl có cấu hình electron là: 1s22s22p63s23p5
⇒ Cl thuộc chu kì 3; nhóm VIIA

Các bạn ơi giúp mình với. Chuyên đề này sáng mai mình phải nộp rồi! Cảm ơn các bạn nhiều!

- Tổng số hàng: 8
- Tổng số cột: 18
- Tổng số nguyên tố hóa học: 118
BẢNG TUẦN HOÀN – TRÁI TIM CỦA HÓA HỌC
Trong thế giới khoa học rộng lớn, hiếm có công trình nào vừa mang tính hệ thống, vừa thể hiện được sự hài hòa giữa trật tự và sáng tạo như bảng tuần hoàn các nguyên tố hóa học. Từ khi được Dmitri Ivanovich Mendeleev công bố năm 1869, bảng tuần hoàn đã trở thành nền tảng của hóa học hiện đại, là “bản đồ” giúp con người khám phá cấu trúc vật chất và bản chất của vũ trụ. Không chỉ là công cụ học tập, bảng tuần hoàn còn là biểu tượng của tri thức nhân loại – nơi hội tụ của logic, tư duy và niềm đam mê khoa học.
1. Lịch sử hình thành và phát triển của bảng tuần hoàn
Trước thế kỷ XIX, con người đã biết đến nhiều nguyên tố như vàng, bạc, đồng, lưu huỳnh… nhưng chưa có cách nào sắp xếp chúng một cách khoa học. Khi số lượng nguyên tố được phát hiện ngày càng tăng, các nhà khoa học bắt đầu nhận thấy giữa chúng có những điểm tương đồng về tính chất. Đó là bước khởi đầu cho hành trình tìm kiếm quy luật trong thế giới nguyên tố.
Đến năm 1869, nhà hóa học người Nga D. I. Mendeleev đã tạo nên bước ngoặt vĩ đại. Ông sắp xếp 63 nguyên tố đã biết dựa theo khối lượng nguyên tử tăng dần và chu kỳ lặp lại của tính chất hóa học. Mendeleev không chỉ hệ thống hóa các nguyên tố đã biết, mà còn dự đoán sự tồn tại và tính chất của những nguyên tố chưa được phát hiện như galli, germani, scandium. Khi các nguyên tố ấy sau này được tìm thấy với đúng đặc điểm ông tiên đoán, bảng tuần hoàn của Mendeleev được công nhận như một kỳ tích khoa học.
Từ đó đến nay, bảng tuần hoàn liên tục được mở rộng và hoàn thiện. Khi cấu trúc nguyên tử được khám phá sâu hơn, các nguyên tố được xếp theo số hiệu nguyên tử (số proton) thay vì khối lượng nguyên tử. Ngày nay, bảng tuần hoàn hiện đại có 118 nguyên tố, là kết quả của hơn 150 năm nỗ lực của nhiều thế hệ nhà khoa học trên toàn thế giới.
2. Cấu trúc và ý nghĩa khoa học của bảng tuần hoàn
Bảng tuần hoàn không chỉ là một danh sách các nguyên tố; nó là một hệ thống thể hiện quy luật tự nhiên. Các nguyên tố được sắp xếp thành chu kỳ (hàng ngang) và nhóm (cột dọc), phản ánh sự biến đổi tuần hoàn của cấu hình electron trong nguyên tử.
Nhờ cấu trúc này, bảng tuần hoàn cho phép ta dự đoán được tính chất của nguyên tố chưa từng gặp, ví dụ như mức độ phản ứng, khả năng tạo hợp chất hay loại liên kết có thể hình thành. Đây chính là sức mạnh dự báo – yếu tố khiến bảng tuần hoàn trở thành công cụ không thể thiếu trong nghiên cứu hóa học.
Ngoài ra, bảng tuần hoàn còn phản ánh xu hướng biến đổi tính chất của các nguyên tố:
Những quy luật ấy là chìa khóa để hiểu bản chất của phản ứng hóa học, giúp người học hóa không chỉ “nhớ công thức” mà còn hiểu sâu về quy luật tự nhiên chi phối thế giới vật chất.
3. Vai trò của bảng tuần hoàn trong khoa học và đời sống
Không có bảng tuần hoàn, hóa học hiện đại sẽ mất đi ngôn ngữ chung của nó. Nhờ có bảng này, các nhà khoa học có thể nghiên cứu, dự đoán và tổng hợp những chất mới. Các ngành như vật lý hạt nhân, sinh học phân tử, y học, vật liệu học, năng lượng tái tạo… đều dựa vào bảng tuần hoàn để phát triển.
Ví dụ, trong y học, hiểu biết về nguyên tố vi lượng (như sắt, kẽm, i-ốt) giúp con người điều chỉnh dinh dưỡng và chữa bệnh. Trong công nghệ, việc phát hiện các nguyên tố đất hiếm – nhóm nguyên tố nằm ở cuối bảng tuần hoàn – đã mở ra kỷ nguyên của điện thoại thông minh, pin lithium và xe điện. Trong năng lượng, các nguyên tố như uranium và thorium là cơ sở cho công nghệ hạt nhân.
Đối với học sinh và sinh viên, bảng tuần hoàn còn là công cụ tư duy. Nó dạy chúng ta cách nhìn thế giới theo trật tự, phát hiện quy luật trong sự đa dạng. Học bảng tuần hoàn không chỉ là ghi nhớ ký hiệu hóa học, mà còn là rèn luyện khả năng tư duy logic và suy luận khoa học.
4. Tính nhân văn và giá trị biểu tượng của bảng tuần hoàn
Ít ai nhận ra rằng bảng tuần hoàn không chỉ là sản phẩm của trí tuệ mà còn mang ý nghĩa nhân văn sâu sắc. Nó thể hiện niềm tin của con người vào sự thống nhất và hợp lý của vũ trụ. Mendeleev đã từng nói: “Nếu tự nhiên ẩn giấu quy luật, thì nhiệm vụ của nhà khoa học là tìm ra quy luật đó.” Bảng tuần hoàn chính là minh chứng rằng vũ trụ không hỗn loạn, mà vận hành theo những quy luật có thể hiểu được.
Hơn thế nữa, bảng tuần hoàn là biểu tượng của sự hợp tác quốc tế trong khoa học. Mỗi nguyên tố mới được phát hiện đều là kết quả của nỗ lực chung của các nhà khoa học từ nhiều quốc gia. Năm 2019, UNESCO đã chọn là Năm Quốc tế của Bảng Tuần Hoàn, nhằm tôn vinh đóng góp của khoa học cho sự phát triển bền vững của nhân loại.
5. Kết luận
Từ những nguyên tố nhỏ bé cấu tạo nên vật chất cho đến những phát minh vĩ đại của thời đại công nghệ, tất cả đều mang dấu ấn của bảng tuần hoàn. Nó là “bản nhạc nền” của hóa học, nơi mà mỗi nguyên tố là một nốt nhạc, cùng hòa quyện thành giai điệu kỳ diệu của vũ trụ.
Đối với người học, hiểu bảng tuần hoàn là hiểu cách mà thế giới được sắp xếp – từ nguyên tử đến cuộc sống. Đối với nhân loại, bảng tuần hoàn là minh chứng cho sức mạnh của trí tuệ con người: dù vũ trụ rộng lớn và phức tạp, con người vẫn có thể tìm ra trật tự trong đó bằng lý trí và niềm đam mê khám phá.
📘 Độ dài: ~1.030 từ.