Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1 , \(n_{Na}=\frac{4,6}{23}=0,2\left(mol\right)\)
\(m_{HCl}=200.2,92\%=5,84\left(mol\right)\) => \(n_{HCl}=\frac{5,84}{36,5}=0,16\left(mol\right)\)
\(2Na+2HCl->2NaCl+H_2\left(1\right)\)
vì \(\frac{0,2}{2}>\frac{0,16}{2}\) => Na dư , HCl hết
dung dịch thu được là dung dịch NaCl
theo (1) \(n_{NaCl}=n_{HCl}=0,16\left(mol\right)\) => \(m_{NaCl}=0,16.58,5=9,36\left(g\right)\)
\(n_{H_2}=\frac{1}{2}n_{HCl}=0,08\left(mol\right)\)
khối lượng dung dịch sau phản ứng là
4,6+200-0,08.2=204,44(g)
\(C_{\%\left(NaCl\right)}=\frac{9,36}{204,44}.100\%\approx4,58\%\)

\(BTNT\left(S\right):n_{SO3}=n_{SO2}=\dfrac{V}{22,4}=\dfrac{5}{14}\left(mol\right)\)
Ta có : \(n_{H2SO4}=\dfrac{9}{25}\left(mol\right)\)
\(\Rightarrow\Sigma n_{H2SO4}=\dfrac{5}{14}+\dfrac{9}{25}=\dfrac{251}{350}\left(mol\right)\)
\(\Rightarrow C\%=\dfrac{m_{H2SO4}}{m_{dd}}.100\%=64,7\%\)

a) Gọi hóa trị của kim loại cần tìm là n
A-----> A+n + ne
S+6 +2e -----> S+4
Áp dụng bảo toàn e : \(n_A=\dfrac{n_{SO_2}.2}{n}=\dfrac{0,6}{n}\)
Ta có: \(\dfrac{19,2}{A}=\dfrac{0,6}{n}\)
Chạy nghiệm theo n:
n=1 --------> A=32 (lọai)
n=2 -------> A=64 ( chọn - Cu)
n=3 ------->A=96 (loại)
Vậy kim loại A là Đồng (Cu)
b) Giả sử phản ứng tạo 2 muối
Gọi x, y lần lượt là số mol KHSO3 và K2SO3
=> \(\left\{{}\begin{matrix}x+y=0,3\\120x+158t=39,8\end{matrix}\right.\)
=> x=0,2, y=0,1 (thỏa mãn)
=> \(n_{KOH}=0,2+0,1.2=0,4\left(mol\right)\)
=> \(CM_{KOH}=\dfrac{0,4}{0,4}=1M\)

Nồng độ mol của dung dịch H 2 SO 4 :
n H 2 SO 4 = n SO 3 = 8/80 = 0,1 mol
Theo phương trình hoá học :
C Mdd H 2 SO 4 = 1000x0,1/250 = 0,4M

\(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
1 1 1 1
0,3 0,3 0,3 0,3
\(n_{Mg}=\dfrac{7,2}{24}=0,3\left(mol\right)\)
a). \(n_{H2}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
⇒\(V_{H2}=n.22,4=0,3.22,4=6,72\left(l\right)\)
b). \(80ml=0,08l\)
\(n_{H2SO4}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
→\(C_M=\dfrac{n}{V}=\dfrac{0,3}{0,08}=3,75\left(M\right)\)
c). \(n_{MgSO4}=\dfrac{0,3.1}{1}=0,3\left(mol\right)\)
\(V_{MgSO4}=n.22,4=0,3.22,4=6,72\left(l\right)\)
→\(C_M=\dfrac{n}{V}=\dfrac{0,3}{6,72}=0,04\left(M\right)\)
d). \(MgSO_4+Ba\left(OH\right)_2\rightarrow Mg\left(OH\right)_2+BaSO_4\downarrow\)
1 1 1 1
0,3 0,3 0,3
\(n_{BaSO4\uparrow}=\dfrac{0,3.1}{1}\)=0,3(mol)
→\(m_{BaSO4\downarrow}=n.M=0,3.233=69,9\left(g\right)\)
\(n_{Ba\left(OH\right)_2}=\dfrac{0,3.1}{1}\)=0,3(mol)
\(\rightarrow V_{ddBa\left(OH\right)_2}=\dfrac{n}{C_M}=\dfrac{0,3}{1,6}=0,1875\left(l\right)\)

Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
a. PTHH: \(Zn+H_2SO_4--->ZnSO_4+H_2\uparrow\left(1\right)\)
b. Theo PT(1): \(n_{Zn}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{Zn}=65.0,3=19,5\left(g\right)\)
c. Theo PT(1): \(n_{H_2SO_4}=n_{Zn}=0,3\left(mol\right)\)
Đổi 300ml = 0,3 lít
\(\Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,3}{0,3}=1M\)
d. PTHH: \(2NaOH+H_2SO_4--->Na_2SO_4+2H_2O\left(2\right)\)
Theo PT(2): \(n_{NaOH}=2.n_{H_2SO_4}=2.0,3=0,6\left(mol\right)\)
\(\Rightarrow m_{NaOH}=0,6.40=24\left(g\right)\)
\(\Rightarrow m_{dd_{NaOH}}=\dfrac{24.100\%}{20\%}=120\left(g\right)\)
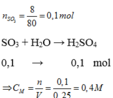
Trước hết, hãy cùng phân tích các phản ứng xảy ra và tính toán nồng độ phần trăm của dung dịch axit thu được. Sau đó, tôi sẽ giải thích tại sao VÌ THẾ3 lại tác dụng với H2CÁC trong H2VÌ THẾ4 mà không trực tiếp với H2VÌ THẾ4.
Phần 1: Tính nồng độ phần trăm của dung dịch axit thu được
1. Tính số mol VÌ THẾ2: Ở đktc (điều kiện tiêu chuẩn), 1 mol khí chiếm 22,4 lít. Số mol VÌ THẾ2=22 , 4l TÔIˊt/mol8 lítTÔIˊt≈0 ,357 mol
2. Phản ứng oxi hóa VÌ THẾ2 thành VÌ THẾ3: 2 S Ớ2( tiếng anh )+CÁC2( tiếng anh )TRONG2CÁC5, t∘2 S Ớ3( tiếng anh ) Theo phương trình, số mol VÌ THẾ3 tạo thành bằng số mol VÌ THẾ2 phản ứng. Vậy, số mol VÌ THẾ3=0 ,357 mol
3. Khối lượng VÌ THẾ3: Khối lượng mol của VÌ THẾ3 là 32+3×16=80 g/mol. Khối lượng VÌ THẾ3=0 ,357 mol×80 g/mol=28 ,56g
4. Khối lượng dung dịch H2VÌ THẾ4 ban đầu: Thể tích dung dịch H2VÌ THẾ4=57 ,2ml Khối lượng riêng D=1 ,5g /ml Khối lượng dung dịch H2VÌ THẾ4=57 ,2ml ×1 ,5g /ml=85 ,8g
5. Khối lượng H2VÌ THẾ4 nguyên chất trong dung dịch ban đầu: Nồng độ phần trăm C %=60% Khối lượng H2VÌ THẾ4 nguyên chất =10060×85 ,8g =51 ,48g
6. Khối lượng H2CÁC trong dung dịch H2VÌ THẾ4 ban đầu: Khối lượng H2CÁC=85 ,8g −51 ,48g =34 ,32g
7. Phản ứng của VÌ THẾ3 với nước: VÌ THẾ3( tiếng anh )+H2O ( l )→H2VÌ THẾ4( một ) Phản ứng này xảy ra với lượng nước có sẵn trong dung dịch H2VÌ THẾ4 ban đầu.
Số mol H2CÁC=18 g/mol34 , 32g ≈1 ,907 mol
So sánh số mol VÌ THẾ3 (0,357 mol) với số mol H2CÁC (1,907 mol). Thấy H2CÁC dư, nên VÌ THẾ3 sẽ phản ứng hết.
Theo phương trình, 1 mol VÌ THẾ3 phản ứng với 1 mol H2CÁC tạo ra 1 mol H2VÌ THẾ4. Vậy, 0,357 mol VÌ THẾ3 sẽ tạo ra 0,357 mol H2VÌ THẾ4.
8. Tính khối lượng H2VÌ THẾ4 mới tạo thành: Khối lượng mol của H2VÌ THẾ4là2×1+32+4×16=98 g/mol. Khối lượngH2VÌ THẾ4 mới tạo thành =0 ,357 mol×98 g/mol=34 ,986g
9. Tính tổng khối lượng H2VÌ THẾ4 trong dung dịch sau phản ứng: Tổng khối lượng H2VÌ THẾ4=H2VÌ THẾ4 ban đầu + H2VÌ THẾ4 mới tạo thành Tổng khối lượng H2VÌ THẾ4=51 ,48g +34 ,986g =86 ,466g
10. Tính khối lượng dung dịch sau phản ứng: Khối lượng dung dịch sau phản ứng = Khối lượng dung dịch H2VÌ THẾ4 ban đầu + Khối lượng VÌ THẾ3 thêm vào Khối lượng dung dịch sau phản ứng =85 ,8g +28 ,56g =114 ,36g
11. Tính nồng độ phần trăm của dung dịch axit thu được: C %=Khcáiˆˊi lượng dung dịch sau phản ứngKhcáiˆˊi lượng H2VÌ THẾ4 tổng×100% C %=114 , 36g 86 , 466 gam×100%≈75 ,61%
Vậy, nồng độ phần trăm của dung dịch axit thu được là khoảng 75,61%.
Phần 2: Giải thích tại sao VÌ THẾ3 tác dụng với H2CÁC trong H2VÌ THẾ4 mà không tác dụng trực tiếp với H2VÌ THẾ4
VÌ THẾ3 là một oxit axit. Khi VÌ THẾ3 được đưa vào dung dịch H2VÌ THẾ4, nó sẽ ưu tiên phản ứng với nước (H2CÁC) có trong dung dịch để tạo thành H2VÌ THẾ4.
VÌ THẾ3( tiếng anh )+H2O ( l )→H2VÌ THẾ4( một )
Lý do:
Tóm lại: VÌ THẾ3 phản ứng với H2CÁC trong dung dịch H2VÌ THẾ4 vì nước có tính nucleophin cao và phản ứng này là phản ứng rất mạnh, thuận lợi. Chỉ khi không còn nước để phản ứng, VÌ THẾ3 mới hòa tan vào H2VÌ THẾ4 tạo thành các dạng oleum (H2VÌ THẾ4⋅n S O3).
Oxit axit ưu tiên tác dụng với nước nha em