Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Vì mỗi nguyên tử N đều có 5 electron ở lớp vỏ ngoài cùng => Cần nhận thêm 3 electron vào lớp vỏ ngoài cùng để có lớp vỏ electron bền vững tương tự khí hiếm
=> Khi 2 nguyên tử N liên kết với nhau, mỗi nguyên tử sẽ góp 3 electron ở tạo ra 3 đôi electron dùng chung

tham khảo
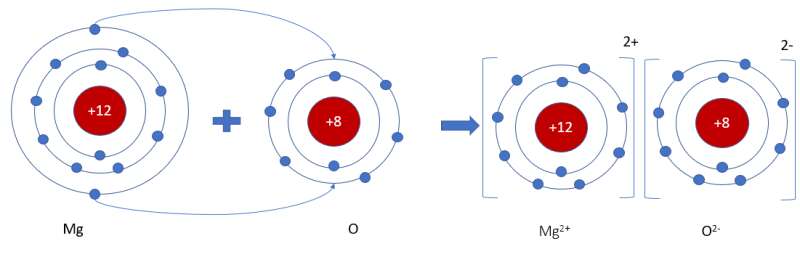
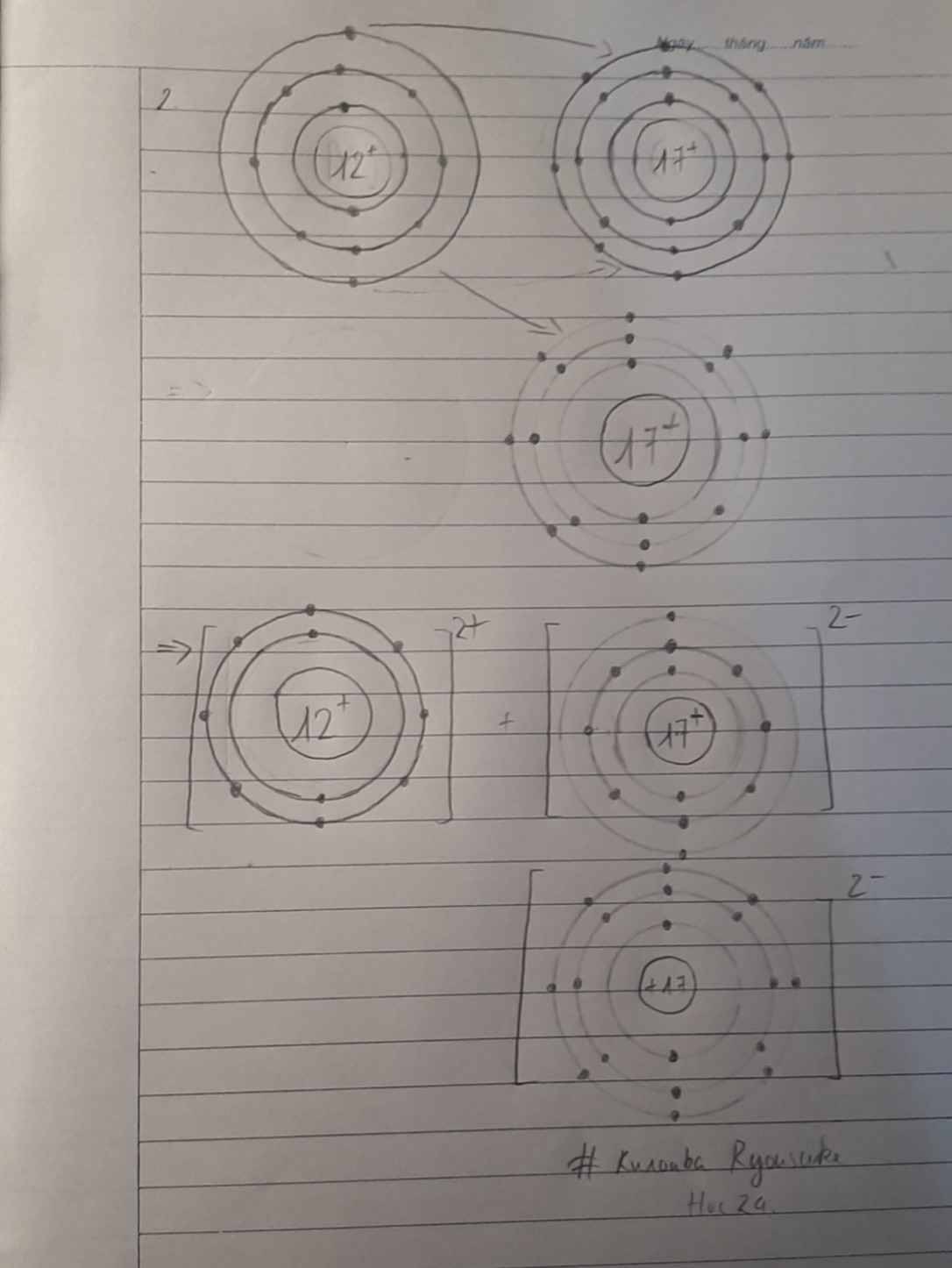
- Nguyên tử Mg (có số hiệu nguyên tử = 12) nhường 2 electron cho O, tạo thành ion Mg2+
- Nguyên tử O (có số hiệu nguyên tử = 8) nhận 2 electron từ Mg, tạo thành ion O2-
=> Ion dương Mg2+ và ion âm O2- mang điện tích trái dấu nên hút nhau, tạo thành liên kết ion
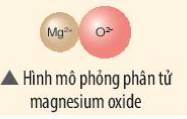
- Sơ đồ mô tả quá trình tạo thành liên kết ion trong phân tử hợp chất magnesium oxide:

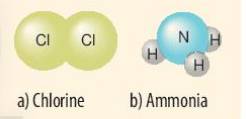
- Xét phân tử khí chlorine
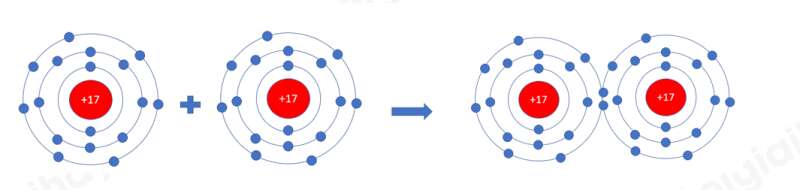
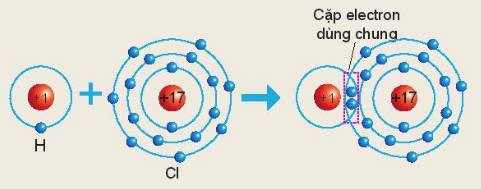
=> Mỗi nguyên tử Cl có 7 electron ở lớp ngoài cùng. Để có cấu trúc electron bền vững của khí hiếm Ar, khi hình thành phân tử chlorine, hai nguyên tử Cl đã liên kết với nhau bằng cách mỗi nguyên tử Cl góp chung 1 electron tạo thành 1 cặp electron dùng chung
- Xét phân tử khí amonia
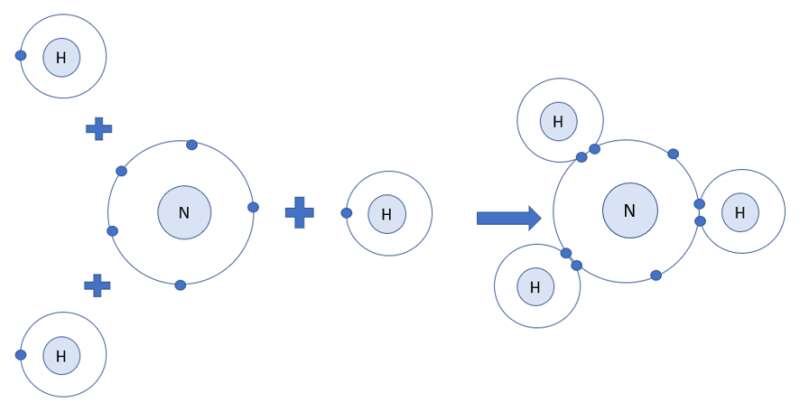
- Nguyên tử H có 1 electron ở lớp ngoài cùng
- Nguyên tử N có 5 electron ở lớp ngoài cùng
=> Nguyên tử H cần thêm 1 electron và N cần thêm 3 electron để đạt cấu hình electron bền vững của khí hiếm
=> Khi 3 nguyên tử H và 1 nguyên tử N liên kết với nhau, mỗi nguyên tử H góp 1 electron và nguyên tử N góp ra 3 electron để tạo ra 3 đôi electron dùng chung

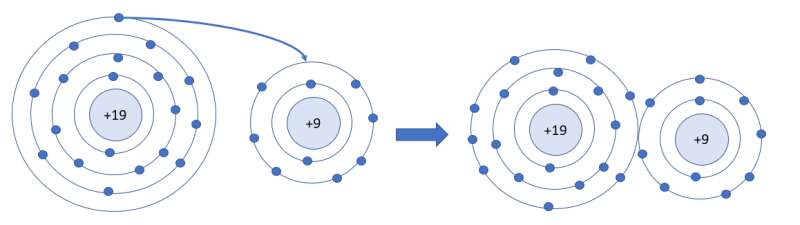
- Ca có 2 electron ở lớp ngoài cùng (giống như nguyên tử Mg) => Dễ dàng cho đi 2 electron ở lớp ngoài cùng để tạo cấu hình electron bền vững của khí hiếm
- O có 6 electron ở lớp ngoài cùng => Dễ dàng nhận thêm 2 electron ở lớp ngoài cùng để tạo cấu hình electron bền vững của khí hiếm
Cái sơ đồ em vẽ vòng e của 2 nguyên tử dùng dấu + xong -> thành 2 vòng e các nguyên tử sát nhau

Nguyên tử `Cl` dùng chung `1` cặp electron với nguyên tử `H`
`->` Trong phân tử muối `HCl,` nguyên tử nguyên tố `Cl` sẽ có hóa trị là `I`.

1. Liên kết trong phân tử CaO
Phân tử CaO (oxit canxi) được hình thành từ canxi (Ca) và oxi (O). Canxi (Ca) là kim loại kiềm thổ có số oxi hóa +2, trong khi oxy (O) là phi kim có số oxi hóa -2. Mối quan hệ giữa chúng là một dạng liên kết ion chứ không phải liên kết cộng hóa trị.
Quá trình hình thành phân tử CaO:
Khi canxi mất hai electron và oxy nhận hai electron, chúng tạo ra liên kết ion mạnh giữa Ca²⁺ và O²⁻ nhờ lực hút tĩnh điện.
Hợp chất CaO là hợp chất ion chứ không phải hợp chất cộng hóa trị. Liên kết giữa Ca và O chủ yếu là liên kết ion, không phải cộng hóa trị.
2. Sơ đồ liên kết trong phân tử CaO
Để vẽ sơ đồ liên kết ion trong CaO:
Dưới đây là một mô phỏng sơ đồ liên kết trong CaO:
Cái này thể hiện sự tạo thành liên kết ion giữa ion Ca²⁺ và ion O²⁻ trong hợp chất CaO.
Hy vọng câu trả lời này giúp bạn hiểu rõ về phân tử CaO và loại liên kết trong đó!