Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Đặt \(\hept{\begin{cases}n_{Al}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{cases}}\)
PTHH : \(2Al+3H_2SO_4-->Al_2\left(SO_4\right)_3+3H_2\) (1)
\(Al+6HNO_3-->Al\left(NO_3\right)_3+3NO_2+3H_2O\) (2)
\(Cu+4HNO_3-->Cu\left(NO_3\right)_2+2NO_2+2H_2O\) (3)
Theo pthh (1) : \(n_{Al}=\frac{2}{3}n_{H_2}=0,2\left(mol\right)\) => \(x=0,2\left(mol\right)\)
Theo ptr (2); (3) : \(n_{NO_2}=3n_{Al}+2n_{Cu}\)
=> \(0,8=0,2\cdot3+2\cdot n_{Cu}\)
=> \(n_{Cu}=0,1\left(mol\right)\)
=> \(a=0,2\cdot27+0,1\cdot64=11,8\left(g\right)\)
b) PTHH : \(NH_3+HNO_3-->NH_4NO_3\) (4)
\(3NH_3+3H_2O+Al\left(NO_3\right)_3-->Al\left(OH\right)_3\downarrow+3NH_4NO_3\) (5)
\(2NH_3+2H_2O+Cu\left(NO_3\right)_2-->Cu\left(OH\right)_2\downarrow+2NH_4NO_3\) (6)
BT Al : \(n_{Al\left(OH\right)_3}=n_{Al}=0,2\left(mol\right)\)
BT Cu : \(n_{Cu\left(OH\right)_2}=n_{Cu}=0,1\left(mol\right)\)
=> \(m\downarrow=m_{Al\left(OH\right)_3}+m_{Cu\left(OH\right)_2}=25,4\left(g\right)\)
c) Gọi tên KL là X .
PTHH : \(2Al\left(NO_3\right)_3-t^o->Al_2O_3+6NO_2+\frac{3}{2}O_2\) (7)
\(Cu\left(NO_3\right)_2-t^o->CuO+2NO_2+\frac{1}{2}O_2\) (8)
\(4NO_2+O_2+2H_2O-->4HNO_3\) (9)
\(3X+4nHNO_3-->3X\left(NO_3\right)_n+nNO+2nH_2O\) (10)
viết ptr rồi, nhưng mik có thắc mắc là cho khí B hấp thụ vô nước => tính đc số mol của hno3, rồi áp vô X là ra, nhưng đề lại cho số mol NO =((( hoặc có thể dùng số mol NO để tính nhưng như thế có hơi thừa ko ? tính ra theo 2 cách thì cx ra 2 kq khác nhau ? ai githich giùm mik, hay mik tính sai hoặc phân tích đề sai nhỉ ?? :D

- Cấu tạo của nguyên tử kim loại.
+ Có số electron hóa trị ít.
+ Trong cùng một chu kì các nguyên tố kim loại có bán kính nguyên tử lớn hơn và điện tích hạt nhân nhỏ hơn so với nguyên tố phi kim trong cùng chu kì.
- Cấu tạo tinh thể kim loại.
+ Kim loại có cấu tạo tinh thể, tinh thể kim loại có cấu tạo mạng.
+ Có 3 loại kiểu mạng tinh thể phổ biến là : Mạng tinh thể luc phương , mạng tinh thể lập phương tâm diện , mạng tinh thể lập phương tâm khối.

-Nguyên tử của hầu hết nguyên tố kim loại đều có ít electron ở lớp ngoài cùng (1,2 hoặc 3e). Thí dụ
Na: [Ne]3s1
Mg: [Ne]3s2
-Cấu tạo tinh thể : Ở nhiệt độ thường, trừ thủy ngân ở thể lỏng, các kim loại khác ở thể rắn và có cấu trúc tinh thể
Trong tinh thể kim loại, nguyên tử và ion kim loại nằm ở những nút của mạng tinh thể. Các electron hóa trị liên kết yếu với hạt nhân nên dễ tách khỏi nguyên tử và chuyển động tự do trong mạng tinh thể.

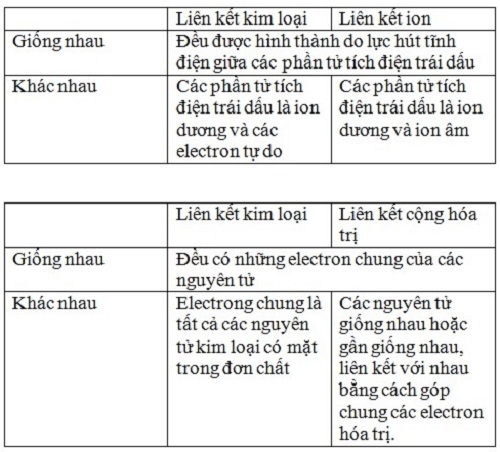
-Liên kết kim loại là liên kết được hình thành giữa các nguyên tử và ion kim loại trong mạng tinh thể do sự tham gia của các electron tự do
-


Đặc điểm tinh thể kim loại:
- Tinh thể kim loại có cấu trúc chặt chẽ, các nguyên tử sắp xếp theo một quy luật nhất định, tạo thành mạng tinh thể.
- Các nguyên tử trong tinh thể kim loại có thể di chuyển một chút, giúp kim loại dễ dàng uốn, kéo thành sợi.
Liên kết kim loại:
- Liên kết kim loại là liên kết giữa các ion kim loại dương và "làn sóng electron tự do" (các electron có thể di chuyển tự do trong mạng tinh thể).
- Liên kết này giúp kim loại có tính dẫn điện, dẫn nhiệt tốt và có độ dẻo, dễ uốn.
Đặc điểm tinh thể kim loại: Cấu trúc: Mạng lưới nguyên tử đều đặn (lập phương tâm khối, lập phương tâm diện, lục giác...). Tính chất: Dẻo, dẫn điện, dẫn nhiệt, có ánh kim. Liên kết kim loại: Bản chất: Chia sẻ electron tự do giữa các ion kim loại dương ("biển electron"). Đặc điểm: Tạo sức liên kết lớn, quyết định tính chất của kim loại.
cấu trúc chặt chẽ ( lập phương tâm khối/tâm diện, lục giác) tính ánh kim, dẻo, dẫn nhiệt và dẫn điện tốt nhờ “biển electron“ tự do
Em ko biết
1. Liên kết kim loại
Liên kết kim loại là loại liên kết được hình thành giữa các nguyên tử và ion kim loại trong mạng tinh thể nhờ sự tham gia của các electron tự do.
• Bản chất: Các electron lớp ngoài cùng của nguyên tử kim loại liên kết lỏng lẻo với hạt nhân, chúng dễ dàng tách ra và di chuyển tự do trong toàn bộ khối kim loại.
• Cơ chế: Các electron tự do này gắn kết các ion dương kim loại lại với nhau, tạo thành một cấu trúc bền vững.
2. Đặc điểm tinh thể kim loại
Mạng tinh thể kim loại bao gồm các ion dương kim loại và nguyên tử kim loại nằm tại các nút mạng, xung quanh là các electron tự do chuyển động hỗn loạn.
Các kiểu mạng tinh thể phổ biến:
Trong chương trình lớp 12, bạn cần nhớ 3 loại cấu trúc chính:
1. Lập phương tâm khối (BCC): Các nguyên tử/ion nằm ở các đỉnh và tâm của hình lập phương (Ví dụ: \bm{Li, Na, K, V, Cr, W}).
2. Lập phương tâm diện (FCC): Các nguyên tử/ion nằm ở các đỉnh và tâm các mặt của hình lập phương (Ví dụ: \bm{Al, Cu, Ag, Au}).
3. Lục phương (HCP): Các nguyên tử/ion xếp chồng lên nhau theo cấu trúc lục giác (Ví dụ: \bm{Be, Mg, Zn}).
Tinh thể kim loại: Trong mạng tinh thể kim loại, các ion dương kim loại nằm ở các nút mạng, còn các electron hóa trị liên kết yếu với hạt nhân nên dễ dàng tách khỏi nguyên tử và chuyển động tự do xung quanh các nút mạng.
Liên kết kim loại: Là liên kết được hình thành giữa các nguyên tử và ion kim loại trong mạng tinh thể do có sự tham gia của các electron tự do.
+ Nguyên tử của hầu hết các nguyên tố kim loại điều có ít electron ở lớp ngoài cùng (1,2,3).
+ Trong cùng chu kì, nguyên tử của nguyên tố kim loại có bán kính nguyên tử lớn hơn và
điện tích hạt nhân nhỏ hơn so với nguyên tử của nguyên tố phi kim.
tính dẻo,tính dẫn nhiệt ,tính dẫn điện và tính ánh kim
đặc điểm tinh thể kim loại và liên kết kim loại
- Cấu tạo: Ở các nút mạng của tinh thể là các nguyên tử và ion dương kim loại.
- Mật độ: Các nguyên tử và ion dương kim loại được sắp xếp một cách hệ thống, khít nhau.
- Electron tự do: Các electron hóa trị liên kết yếu với hạt nhân nên dễ dàng tách ra khỏi nguyên tử, chuyển động tự do trong toàn bộ mạng lưới tinh thể, tạo thành một "biển electron" (hoặc đám mây electron).
- Các kiểu mạng phổ biến: Tùy vào loại kim loại mà có các kiểu mạng khác nhau như: Lập phương tâm khối, lập phương tâm diện và lục phương.
2. Liên kết kim loại Liên kết kim loại là loại liên kết hóa học đặc trưng giữ cho các nguyên tử kim loại gắn kết với nhau trong tinh thể.- Các nút mạng: Tại các nút mạng là các nguyên tử và ion dương kim loại.
- Các electron tự do: Các electron hóa trị tách khỏi nguyên tử, chuyển động tự do trong toàn bộ mạng tinh thể, tạo thành một "biển electron".
- Các kiểu mạng phổ biến: Có 3 kiểu mạng tinh thể kim loại chính:
- Lập phương tâm diện: (Ví dụ: 𝐶𝑢 , 𝐴𝑔 , 𝐴𝑢 , 𝐴𝑙 , . . .) các nguyên tử/ion chiếm các đỉnh và tâm các mặt của hình lập phương.
- Lập phương tâm khối: (Ví dụ: 𝐿𝑖 , 𝑁𝑎 , 𝐾 , 𝑉 , 𝑀𝑜 , . . .) các nguyên tử/ion chiếm các đỉnh và tâm của hình lập phương.
- Lục phương: (Ví dụ: 𝐵𝑒 , 𝑀𝑔 , 𝑍𝑛 , . . .) các nguyên tử/ion sắp xếp theo cấu trúc lục giác xếp khít.
2. Liên kết kim loại- Cấu trúc tinh thể: Kim loại có cấu trúc tinh thể vững chắc, trong đó các nguyên tử hoặc ion kim loại được sắp xếp theo một trật tự tuần hoàn, lặp đi lặp lại trong không gian theo một mạng tinh thể nhất định.
- Loại mạng tinh thể: Các mạng tinh thể phổ biến bao gồm lập phương tâm khối, lập phương tâm diện, và lục phương.
Liên kết kim loại*Tinh thể kim loại*
- Tinh thể kim loại là cấu trúc tinh thể của kim loại, trong đó các nguyên tử kim loại được sắp xếp theo một trật tự nhất định.
- Các nguyên tử kim loại thường được sắp xếp theo cấu trúc lập phương tâm diện (fcc), lập phương tâm khối (bcc) hoặc cấu trúc lục phương xếp chặt (hcp).
- Trong tinh thể kim loại, các nguyên tử kim loại được liên kết với nhau bằng liên kết kim loại.
*Liên kết kim loại*
- Liên kết kim loại là loại liên kết hóa học giữa các nguyên tử kim loại, trong đó các electron tự do di chuyển tự do trong tinh thể kim loại.
- Liên kết kim loại được hình thành do sự chồng lấp của các orbital nguyên tử kim loại, tạo ra một "biển" electron tự do.
- Các tính chất của liên kết kim loại:
- *Tính dẫn điện*: kim loại dẫn điện tốt do sự di chuyển của electron tự do.
- *Tính dẫn nhiệt*: kim loại dẫn nhiệt tốt do sự di chuyển của electron tự do.
- *Tính dẻo*: kim loại có tính dẻo do các nguyên tử kim loại có thể di chuyển tương đối với nhau.
- *Tính sáng*: kim loại có tính sáng do sự phản xạ của ánh sáng trên bề mặt kim loại.
Liên kết kim loại là yếu tố quan trọng quyết định các tính chất của kim loại, và nó đóng vai trò quan trọng trong nhiều ứng dụng công nghiệp và đời sống.
Đặc điểm tinh thể kim loại
- cấu tạo tinh thể kim loại được cấu tạo từ các nguyên tử và ion kim loại ở các nút mạng tinh thể
- sự phân bố các electron hóa trị di chuyển tự do trong toàn bộ mạng tinh thể , tạo thành một " biển electron"
- các kiểu mạng tinh thể kim loại thường có 3 kiểu mạng tinh thể phổ biến : lập phương tâm diện , lập phương tâm khối và lực phương
Đặc điểm liên kết kim loại
- Định hướng liên kết kim loại là liên kết được hình thành do sự hút tĩnh điện giữa các ion dương kim loại ở các nút mạng và các electron tự do di chuyển trong toàn bộ mạng tinh thể
- Bản chất liên kết này không mang tính định hướng có nghĩa là lực hút giữa các ion dương và các đám mây electron tự do
- phạm vi liên kết kim loại tồn tại trong các đơn chất kim loại và một số hợp kim
Các tinh thể kim loại có cấu trúc chặt chẽ, các nguyên tử/cation kim loại được sắp xếp theo một trật tự xác định. Liên kết kim loại được hình thành bởi lực hút tĩnh điện giữa các cation kim loại và các electron hóa trị tự do.
1. Đặc điểm tinh thể kim loại
-Cấu tạo chung:
Kim loại ở trạng thái rắn có cấu trúc tinh thể, trong đó các ion dương kim loại nằm tại các nút mạng tinh thể, còn các electron hóa trị chuyển động tự do trong toàn bộ khối kim loại.
-Mạng tinh thể phổ biến:
Có 3 kiểu mạng tinh thể kim loại thường gặp:
-Lập phương tâm khối (BCC): ví dụ Fe (ở nhiệt độ thường), Na
-Lập phương tâm diện (FCC): ví dụ Al, Cu, Ag
-Lục phương (HCP): ví dụ Mg, Zn
-Đặc điểm nổi bật:
-Các ion dương sắp xếp trật tự, chặt chẽ
-Có “biển electron tự do” chuyển động khắp tinh thể
-Cấu trúc này giúp kim loại có:
-Tính dẫn điện, dẫn nhiệt tốt
-Tính dẻo (dễ dát mỏng, kéo sợi)
-Ánh kim
2. Liên kết kim loại
-Khái niệm:
Liên kết kim loại là lực hút tĩnh điện giữa các ion dương kim loại và các electron tự do trong mạng tinh thể.
-Bản chất:
+Các nguyên tử kim loại nhường electron hóa trị → trở thành ion dương
+Electron bị tách ra không thuộc riêng nguyên tử nào mà tạo thành đám mây electron chung
-Đặc điểm của liên kết kim loại:
+Không định hướng → giúp kim loại dễ biến dạng mà không bị vỡ
+Bền vững nhờ lực hút giữa ion dương và electron
+Tạo nên các tính chất đặc trưng:
+Dẫn điện tốt (electron di chuyển tự do)
+Dẫn nhiệt tốt
+Có tính dẻo và dễ gia công
- Cấu tạo: Ở trạng thái rắn, các kim loại có cấu tạo mạng tinh thể. Tại các nút của mạng tinh thể là các nguyên tử kim loại hoặc các ion dương kim loại.
- Cấu trúc mạng: Các mạng tinh thể kim loại phổ biến bao gồm lập phương tâm khối (như Fe, Na, K), lập phương tâm diện (như Al, Cu, Au) và lục phương (như Mg, Zn).
- Electron tự do: Các electron hóa trị trong tinh thể kim loại không gắn chặt với nguyên tử mà di chuyển tự do trong toàn bộ mạng tinh thể.
Liên kết kim loại- Bản chất: Là lực hút tĩnh điện giữa các cation (ion dương) kim loại tại các nút mạng và các electron tự do chuyển động hỗn loạn xung quanh chúng.
- Cơ chế: Các nguyên tử kim loại dễ dàng nhường electron hóa trị để trở thành ion dương. Các electron này không thuộc về riêng một nguyên tử nào mà gắn kết cả khối tinh thể lại với nhau.
2. Đặc điểm tinh thể kim loại Tinh thể kim loại có cấu trúc đặc biệt quyết định các tính chất vật lý đặc trưng của chúng.Cấu trúc mạng tinh thể kim loại dựa trên sự sắp xếp tuần hoàn của các cation, trong khi liên kết kim loại là kết quả của sự tương tác tĩnh điện giữa các cation này và đám mây electron tự do.
Các ion dương kim loại nằm tại các nút mạng tinh thể, trong khi các electron hóa trị chuyển động tự do xung quanh. Liên kết kim loại được hình thành bởi lực hút tĩnh điện giữa các electron tự do này và các ion dương kim loại.
Đặc điểm tinh thể kim loại (Mạng tinh thể) Cấu tạo: Bao gồm các cation kim loại ( ) nằm ở các nút mạng tinh thể. Sự phân bố electron: Các electron hóa trị (lớp ngoài cùng) tách rời khỏi nguyên tử, di chuyển tự do trong toàn bộ mạng lưới, tạo thành "biển" electron. Các kiểu mạng: Chủ yếu có 3 kiểu mạng tinh thể phổ biến: lập phương tâm khối, lập phương tâm diện và lục phương (trong đó lập phương tâm diện và lục phương là các kiểu đóng khít nhất). Tính chất vật lý: Tính dẻo: Dễ rèn, kéo sợi, dát mỏng do các cation kim loại có thể trượt lên nhau mà không bị phá vỡ cấu trúc nhờ sự linh động của biển electron. Tính dẫn điện/nhiệt: Các electron tự do mang điện tích và nhiệt năng di chuyển từ nơi có mật độ electron/nhiệt độ cao đến nơi thấp hơn. Ánh kim: Các electron tự do phản xạ ánh sáng nhìn thấy, tạo vẻ sáng bóng. 2. Đặc điểm liên kết kim loại Bản chất: Liên kết kim loại là lực hút tĩnh điện giữa các cation dương kim loại ( ) tại các nút mạng và "biển" electron tự do chuyển động xung quanh chúng. Phạm vi: Liên kết kim loại được hình thành giữa các nguyên tử kim loại (hoặc hợp kim) và có tính chất không định chỗ (electron tự do di chuyển khắp tinh thể). Tác dụng: Liên kết các cation kim loại lại với nhau, đảm bảo cấu trúc mạng lưới ổn định và bền vững. Đặc điểm đặc trưng: Sức liên kết lớn (quyết định độ cứng) và khả năng "keo dính" linh hoạt
Đặc điểm tinh thể kim loại là các ion dương nằm ở nút mạng và electron tự do di chuyển xung quanh, còn liên kết kim loại là lực hút tĩnh điện giữa chúng.
cấu trúc chặt chẽ, tính dẻo, ánh kim, dẫn điện và dẫn nhiệt tốt, phổ biến là các kiểu mạng lập phương tâm khối, tâm mặt hoặc lục giác.
Tinh thể kim loại gồm các cation kim loại nằm tại nút mạng, liên kết với nhau bằng lực hút tĩnh điện với "biển" electron tự do di chuyển trong mạng
Liên kết kim loại
Trong tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hoá trị tự do với các ion dương kim loại ở các nút mạng.
Liên kết ion
Đặc điểm tinh thể kim loại
Đặc điểm liên kết kim loại