Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án B
Vì công thức khí với hidro của R là RH3
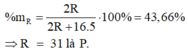
Vậy công thức oxit cao nhất của R là P2O5.

Đáp án B
Vì công thức khí với hidro của R là RH3
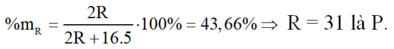
Vậy công thức oxit cao nhất của R là P2O5.

Hớp chất khí với H của R có CT là RH3
=> CT oxit cao nhất là R2O5
Có \(\dfrac{2.M_R}{2.M_R+16.5}.100\%=43.66\%=>M_R=31\left(P\right)\)

Gọi CTHH của R với oxi là: R2O3
Theo đề, ta có: \(\%_{O_{\left(R_2O_3\right)}}=\dfrac{16.3}{NTK_R.2+16.3}.100\%=56,34\%\)
=> \(NTK_R\approx19\left(đvC\right)\)
=> R là flo (F)
=> CTHH của R và H là: FH3
CTHH của R và O là: F2O3

CTHH của oxit : RO
a) \(Tacó:\%R=\dfrac{R}{R+16}=60\%\\ \Rightarrow R=24\left(Mg\right)\)
b) - MgCl2 : Liên kết ion
- Trong phân tử MgO, hiệu độ âm điện của O và Mg là 3,44 − 1,31 = 2,13, liên kết giữa O và Mg là liên kết ion.
c) \(n_{MgCO_3}=0,15\left(mol\right);n_{HCl}=0,4\left(mol\right)\\ MgCO_3+2HCl\rightarrow MgCl_2+H_2O+CO_2\\ LTL:\dfrac{0,15}{1}< \dfrac{0,4}{2}\Rightarrow HCldư\\ n_{MgCl_2}=n_{MgCO_3}=0,15\left(mol\right)\\ n_{HCl\left(dư\right)}=0,4-0,15.2=0,1\left(mol\right)\\ \Rightarrow CM_{MgCl_2}=\dfrac{0,15}{0,2}=075M\\ CM_{HCl}=\dfrac{0,1}{0,2}=0,5M\)

a) CT hợp chất khí cao nhất : RH3
=> CT hợp chất với O : R2O5
%R = 2R/(2R + 16*5) *100% = 43.66%
<=> R = 31
=> R : P
b)
R thuộc nhóm VII A => R có hóa trị cao nhất với O là VII
=> CT hợp chất khí với H : RH
%H = 1/(R+1) *100% = 39/50%
=> R = 127
=> R là : I
c) R thuộc nhóm VII A => R có hóa trị cao nhất với O là: VII
=> CT : R2O7
%R = 2R/(2R + 16*7) *100% = 38.79%
=> R = 35.5
=> R là : Cl
d) Oxit cao nhất là : R2O5
=> CT hợp chất khí với H : RH3
%H = 3/(R+3) *100% = 17.65%
=> R = 14
=> R là : N
a)
công thức hợp chất của R với H là RH3 => công thức oxit cao nhất của R là R2O5
ta có : 2R / 2R + 16.5 = 43,66%
=> R= 31 => photpho
c) CTHH:R2O7
R chiếm 38.79%
Suy ra
\(\frac{2R}{2R+16.7}=\)0,3879
=>2R=0,,7758R+42,44
=>1,22R=43,44
=>R=36 Xem lại đề
d)
R2O5
công thức với hidro là : RH3
Ta có : R/R+3=0,9118⇒R=31 là P
f) R+2HCl--->RCl2+H2
n\(_{H2}=\frac{4,48}{22,4}=0,2\left(mol\right)\)
Theo pthh
n\(_R=n_{H2}=0,2\left(mol\right)\)
M\(_M=\frac{13}{0,2}=65\left(Zn\right)\)
e)
KX + AgNO3 --> KNO3 + AgX
39+X__________________108+X
4.76___________________7.52
<=> 7.52(39+X) = (108+X)4.76
=> X = 80 (Br)
f) Sửa đề : 4.48 (l) H2
nH2 = 0.2 mol
R + 2HCl --> RCl2 + H2
0.2_______________0.2
MR = 13/0.2 = 65
=> R là : Zn
g) nHCl = 0.06 mol
AOH + HCl --> ACl + H2O
0.06____0.06
A + H2O --> AOH + 1/2H2
0.06________0.06
MA = 1.38/0.06 = 23
=> A là : Na
h) CT hợp chất khí với H : RH3
=> CT hợp chất cao nhất với O : R2O5
%R = 2R/(1R + 16*5) *100% = 25.92%
=> R = 14
R là : N
\(\text{a) RH3}\Rightarrow\text{R ở nhóm VA}\)
Ta có:
\(\text{2xR/(2R+16x5)=43,66%}\)
\(\Rightarrow\text{R=31}\left(P\right)\)
\(\text{b)CTHH là RH2}\)
%H là bao nhiêu vậy
\(\text{c) CTHH oxit là R2O7}\)
2R/(2R+16x7)=38,79%
=>R=35,5
\(\text{R là Cl}\)
d) R2O5=>R ở nhóm VA
\(\Rightarrow\text{CTHH của oxit là RH3}\)
\(\Rightarrow\text{MRH3=3/17,65%=17}\)
=>R =14 R là Nito
e) KX + AgNO3 -> AgX + KNO3
\(\text{Ta có: nKX=4,76/(39+X)}\)
Kết tủa là AgX -> nAgX=7,52/(108+X)
Theo ptpu: nKX=nAgX -> X=80 -> Br -> Muối là KBr.
f) Phản ứng: R + 2HCl -> RCl2 + H2
\(\text{Ta có: nH2=4,48/22,4=0,2 mol}\)
Theo ptpu: nR=nH2=0,2 mol -> MR=13/0,2=65 -> R là Zn (kẽm)
g) R + H2O -> ROH + 1/2H2
ROH + HCl -> RCl +H2O
\(\text{Ta có: nHCl=0,06.1=0,06 mol}\)
Theo ptpu: nR=nROH=nHCl=0,06 mol -> M R=1,38/0,06=23 -> Na
\(\text{h) Hợp chất với H của R là RH3 có 2 trường hợp xảy ra }\)
R nhóm IIIA -> oxit là R2O3 -> 2R/(2R+16.3)=25,92% -> R=8,4 -> loại
R nhóm VA -> oxit là R2O5 -> 2R/(2R+16.5)=25,92% ->R =14 -> N (nito)
Cảm ơn bạn.