
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


F O Cl N
Độ âm điện: 3,98 3,44 3,16 3,14
Nhận xét: tính phi kim giảm dần.
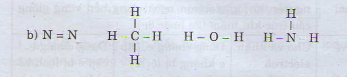
N2 CH4 H2O NH3
Hiệu độ âm điện: 0 0,35 1,24 0,84
Phân tử N2, CH4 có liên kết cộng hóa trị không phân cực. Phân tử H2O có liên kết cộng hóa trị phân cực mạnh nhất trong dãy.

Chọn D
Trong phản ứng trao đổi, số oxi hóa của các nguyên tố không thay đổi.
A sai vì là phản ứng hóa hợp.
B và C sai vì là phản ứng oxi hóa – khử.

Trong phản ứng hóa học , phản ứng nào có sự chuyển dịch electron điều liên quan đến "điện hóa". Khi này phản ứng nào có chênh lệch thế điện hóa (ΔE)càng lớn càng dễ dàng phán ứng, tức ưu tiên xảy ra trước.
Vậy thì trong hệ có bao nhiêu cặp có thể sinh ra chênh lệch thế điện hóa cứ liệt kê ra. Ở mỗi cặp phải có một tác nhân cho electron và một tác nhân nhận electron thì mới tạo thành một phản ứng điện hóa. Trường hợp này có 3 cặp :
Cặp 1 : Fe3+ + 1 e --> Fe2+ Eo = 0.771
...........Zn - 2e --> Zn2+ Eo = -0.763
=> ΔE = 0.771 - (-0.763) = 1.534
Cặp 2 : Fe2+ + 2 e --> Fe Eo = -0.44
............Zn - 2e ---> Zn2+ Eo = -0.763
=> ΔE = -0.44 - (-0.763) = 0.296
Cặp 3 : 2H+ + 2 e ---> H2 Eo = 0
............ Zn - 2 e --> Zn2+ Eo = -0.763
=> ΔE = 0 - (-0.763) = 0.763
Xếp từ lớn tới bé : Cặp 1 > Cặp 3 > Cặp 2
Vậy cặp 1 xảy ra trước nhất, khi không còn tác nhân đảm bảo cho cặp 1 , đến cặp 3, tương tự cho đến cặp 2 . Nghĩa là Zn phản ứng với Fe3+ để tạo thành Fe2+, sau đó hết Fe3+ mà vẫn còn kẻm thì Zn tác dụng với H+ tạo thành H2 , khi hết H+ mà vẫn còn Zn, Zn tác dụng với Fe2+ tạo thành Fe. Bạn đã nghĩ đúng.
~~~~~~~~~~~~~~~~~~~
Bài giải trên chỉ đúng trong trường hợp tất cả các tác nhân điều có nồng độ 1 mol/l
Nếu nồng độ các tác nhân khác nhau , lúc này phải tích chênh lệch thế điện hóa cân bằng, ký hiệu Ecb. Với Ecb được tính bằng công thức :
Ecb = Eo + 0.059/n . log ([Ox]/[Kh])
trong đó n là cái số trong phương trình này: Kh - n e --> Ox
[Ox] - nồng độ tác nhân Oxi hóa
[Kh] - nồng độ tác nhân khử
Theo công thức trên khi [Ox] = [Kh] = 1 mol/l thì log([Ox]/[Kh]) = log(1) = 0 vậy Ecb = Eo

- 1s1 s1𝑠: ↑↓up arrow down arrow↑↓
- 2s2 s2𝑠: ↑↓up arrow down arrow↑↓
- 2p2 p2𝑝:
a) Viết cấu hình electron của nguyên tử Oxygen
Ta có Z = 8 vì nguyên tử trung hòa về điện nên => số e = 8
Cấu hình: 1s²2s²2p⁴
b) Viết cấu hình electron của theo ô orbital của Oxygen
Ta có cấu hình: 1s²2s²2p⁴
=> 1s 2s 2p
|↑↓| |↑↓| |↑↓|↑ |↑ |

Điều chế MgCl2 bằng :
- Phản ứng hoá hợp : Mg + Cl2 —-> MgCl2
- Phản ứng thế : Mg + CuCl2 —-> MgCl2 + Cu
- Phản ứng trao đổi : Mg(OH)2 + 2HCl —-> MgCl2 + 2H2O
Điều chế MgCl\(_2\)bằng
- Phản ứng hóa hợp Mg + \(Cl_2\) —-> \(MgCl_2\)
-Phản ứng thế Mg + \(CuCl_2\) —-> \(MgCl_2\) + Cu
-Phản ứng trao đổỉ \(Mg\left(OH\right)_2\) + 2HCl —-> \(MgCl_2\) + 2\(H_2O\) .
Chào bạn, diễn đàn ưu tiên giải đáp các câu hỏi học tập cụ thể. Bạn hãy đăng câu hỏi chi tiết để được hỗ trợ tốt hơn nhé!