Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B.
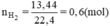
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2 ↓
Al2O3 + 2NaOH → 2NaAlO2 + H2O
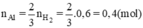
⇒ mAl = 27.0,4 = 10,8 (gam); mAl2O3 = 31,2 - 10,8 = 20,4 (gam).

Gọi a và b lần lượt là số mol của nhôm và của nhôm nitrat.
mX=mnhôm nitrat ⇔ 27a+213b=\(\dfrac{a+b}{2}\).102 ⇔ b=\(\dfrac{4}{27}\)a.
BTe: 3nnhôm=3nNO=3.0,81 ⇒ nnhôm=a=0,81 mol ⇒ b=nnhôm nitrat=0,12 mol.
Rắn khan trong Y chỉ chứa Al(NO3)3 (0,81+0,12=0,93 (mol)) với khối lượng là 0,93.213=198,09 (g).
Chọn B.

Gọi a,b,c,d lần lượt là số mol của Al,Mg,Fe,Zn
Số mol H2 thu được n = = 0,065
Phương trình phản ứng khi cho hỗn hợp tác dụng với axit
Al Al3+ + 3e
a mol 3a mol
Mg Mg2+ + 2e
b mol 2b mol
Fe Fe2+ + 2e
c mol 2c mol
Zn Zn2+ + 2e
d mol 2d mol
2H+ +2e H2
2.0,065 0,065
ta có phương trình :
3a +2b + 2c + 2d =2.0,065 =0,13 (1)
Khi cho hỗn hợp trên tác dụng với clo thu được muối.như vậy khối lượng Clo có trong muối là : mCl2 = m+ 4,97 –m =4,97 gam
Suy ra nCl2 = 0,07 mol
Tuong tự như phương trình phản ứng trên ta có phương trình toán học
3a +3b + 2c + 2d =0,07.2 =0,14 (2)
Lấy (2) – (1) ta có : b=0,01 .suy ra khối lượng Fe = 0,01 . 56 = 0,56 g

Căn cứ vào các tính chất của các halogen ta thấy chỉ có C3H7Cl phản ứng được với dung dịch NaOH đun nóng. Đặt công thức của Y là RCl, phương trình phản ứng :
C3H7Cl + NaOH = C3H7OH + NaCl (1)
mol: x x
AgNO3 + NaCl = AgCl + NaNO3 (2)
mol: x x
Theo (1), (2) và giả thiết ta có :
nC3H7Cl = nNaCl = nAgCl = 1,435/143,5 = 0.01 mol;
mC6H5Cl = 1,91 - 0,01.78,5 = 1,125 gam.

đề cho có bị sai số liệu không?
Thể tích khí Cl2 sao lại là 13,32(l) ????
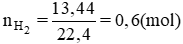
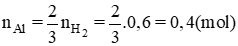
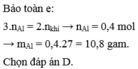
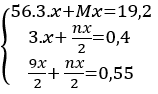
PTHH: 2Al + 2NaOH + 2H2O ===> 2NaAlO2 + 3H2 (1)
Al2O3 + 2NaOH ===> 2NaAlO2 + H2O (2)
Ta có: nH2 = \(\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Theo (1), nAl = \(\dfrac{0,6\cdot2}{3}=0,4\left(mol\right)\)
=> \(\left\{{}\begin{matrix}m_{Al}=0,4\cdot27=10,8\left(gam\right)\\m_{Al2O3}=31,2-10,8=20,4\left(gam\right)\end{matrix}\right.\)
=> Chọn đáp án B là đúng
Chọn B.
nH2 = 0,6 (mol).
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2↑
0,4 0,6 (mol)
Al2O3 + 2NaOH → 2NaAlO2 + H2O
=> mAl = 27.0,4 = 10,8 (gam)
mAl2O3 = 31,2 -10,8 = 20,4 (gam).
Cho 31,2 gam hỗn hợp bột Al và Al2O3 tác dụng hết với dung dịch NaOH dư thu được 13,44 lít H2 ở đktc. Khối lượng từng chất trong hỗn hợp ban đầu lần lượt là
A.16,2 gam và 15 gam.
B. 10,8 gam và 20,4 gam.
C. 6,4 gam và 24,8 gam.
D. 11,2 gam và 20 gam.
\(2Al\left(x\right)+2H_2O+2NaOH\rightarrow3H_2\left(1,5x\right)+2NaAlO_2\)
\(Al_2O_3+2NaOH\rightarrow H_2O+2NaAlO_2\)
Gọi số mol của Al và Al2O3 lần lược là x, y
\(\Rightarrow27x+102y=31,2\left(1\right)\)
\(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
\(\Rightarrow1,5x=0,6\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}27x+102y=31,2\\1,5x=0,6\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,4\\y=0,2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m_{Al}=0,4.27=10,8\\m_{Al_2O_3}=0,2.102=20,4\end{matrix}\right.\)
Chọn B
Al + NaOH + H2O --> Na AlO2 + 3/2 H2
..........0,4......................................................(0,6)
=> m_Al = 0,4 . 27 = 10,8g
=> m_Al2O3 = 31,2 - 10,8 = 20,4g
@Cẩm Vân Nguyễn Thị
@Cẩm Vân Nguyễn Thị
Ghét gì mà kêu cô vô thế b Kẹo gum :v